题目内容
实验室中模拟纯碱工业制法,进行了如下三步实验:①将CO2、NH3通入H2O中制得NH4HCO3,②NH4HCO3和饱和食盐水反应生成小苏打,③将小苏打制成纯碱。
(1)步骤①先通入水中的气体是______。析出NH4HCO3的反应有两步,第二步反应的离子方程式为____________________。
(2)步骤②生成了含少量NaCl的小苏打,现用滴定法测定其中NaHCO3的含量。过程为:称取一定质量样品,配成250mL溶液,取出25.00mL用0.1000mol/L的盐酸滴定。实验中所写的定量仪器除滴定管外,还有_______、_______。所用的指示剂是______________。
(3)步骤②生成了含少量NaHCO3的纯碱。若用重量法(限用试剂:稀盐酸)测定其中Na2CO3含量,请设计实验方案:_______________________。若该样肠中NaHCO3含量的准确值为99.5%,而上述实验结果为97.6%,则测定的相等误差为___________,可能造成该实验误差的原因是________________。
 阅读快车系列答案
阅读快车系列答案下列各组澄清溶液中离子能大量共存,且加入(或滴入)X试剂后发生反应的离子方程式书写正确的是( )
选项 | 离子组 | X试剂 | 离子方程式 |
A | K+、Na+、ClO-、SO42- | 少量SO2 | SO2+ClO-+H2O=SO42-+Cl-+2H+ |
B | NH4+、Fe3+、Br-、SO42- | 过量H2S | 2Fe3++H2S=2Fe2++S↓+2H+ |
C | NH4+、Na+、Fe3+、AlO2- | 过量铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
D | K+、Na+、 HCO3-、AlO2- | 少量HCl | H++AlO2-+H2O=Al(OH)3↓ |
A. A B. B C. C D. D
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
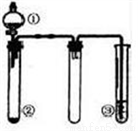
选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
现有部分元素的性质或原子结构信息如表,据此回答下列问题:
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有________种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________。
(2)元素Y的价电子排布图为________________,元素Y与元素T相比,电负性较大的是________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________,稳定性比较:W3+________W2+(填“>”或“<”),原因是__________________________________________________________________________。



