题目内容
下列实验对应的结论正确的是( )
A、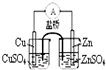 如图能组成Zn、Cu原电池 |
B、 如图能证明非金属性C>Si |
C、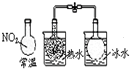 如图说明反应2NO2?N2O4,△H>0 |
D、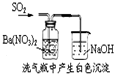 如图白色沉淀为BaSO3 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.Zn比Cu活泼,发生Zn与硫酸铜的电池反应;
B.发生强酸制弱酸的反应,可知碳酸的酸性大于硅酸;
C.二氧化氮为红棕色气体,利用颜色的变化可判断焓变;
D.二氧化硫与硝酸钡发生氧化还原反应.
B.发生强酸制弱酸的反应,可知碳酸的酸性大于硅酸;
C.二氧化氮为红棕色气体,利用颜色的变化可判断焓变;
D.二氧化硫与硝酸钡发生氧化还原反应.
解答:
解:A.Zn比Cu活泼,发生Zn与硫酸铜的电池反应,图中装置可形成原电池,故A正确;
B.发生强酸制弱酸的反应,可知酸性为盐酸>碳酸>硅酸,由非金属性越强其最高价氧化物的水化物酸性越强可知,非金属性C>Si,故B正确;
C.二氧化氮为红棕色气体,热水中颜色的深,则说明反应2NO2?N2O4,△H<0,故C错误;
D.二氧化硫与硝酸钡发生氧化还原反应,二氧化硫为还原剂,生成硫酸钡白色沉淀,故D错误;
故选AB.
B.发生强酸制弱酸的反应,可知酸性为盐酸>碳酸>硅酸,由非金属性越强其最高价氧化物的水化物酸性越强可知,非金属性C>Si,故B正确;
C.二氧化氮为红棕色气体,热水中颜色的深,则说明反应2NO2?N2O4,△H<0,故C错误;
D.二氧化硫与硝酸钡发生氧化还原反应,二氧化硫为还原剂,生成硫酸钡白色沉淀,故D错误;
故选AB.
点评:本题考查化学实验方案的评价,为高频考点,侧重分析能力与实验能力的综合考查,把握原电池原理、酸性比较、平衡移动及氧化还原反应为解答的关键,注意实验的评价性和操作性分析,题目难度不大.

练习册系列答案
相关题目
在2A+B═3C+4D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol?L-1?s-1 |
| B、v(B)=0.3 mol?L-1?s-1 |
| C、v(C)=0.7 mol?L-1?s-1 |
| D、v(D)=1 mol?L-1?s-1 |
1mol下列物质完全燃烧时,消耗O2的量最大的一组是( )
| A、C2H6 |
| B、C2H5OH |
| C、C2H4 |
| D、CH3COOH |
X、Y为短周期元素,X原子中K、L、M各电子层的电子数之比为1:4:1,Y原子比X原子少3个电子,下列叙述正确的是( )
| A、X、Y形成化合物表示为X2Y |
| B、X、Y形成的化合物中所含离子都是10电子微粒 |
| C、Y位于周期表中第ⅦA族,其最高正化合价为+7 |
| D、X原子半径小于Y的原子半径 |
下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
| A、只有②③④⑤ | B、只有①②⑤ |
| C、只有②③⑤ | D、全部 |
下列实验操作能达到实验目的是( )
A、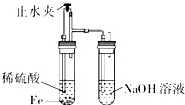 氢氧化亚铁的制备 |
B、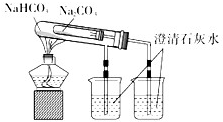 比较Na2CO3、NaHCO3的热稳定性 |
C、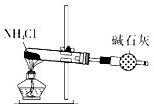 实验室制备少量氨气 |
D、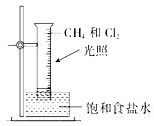 甲烷的取代反应 |
下列有关氯元素的单质及化合物的性质说法正确的是( )
| A、液氯和氯水是纯净物,而漂白粉是混合物 |
| B、氯气可用作消毒剂和漂白剂,是因为次氯酸具有强氧化性 |
| C、实验室制取氯气时,可用饱和Na2CO3溶液除去其中的HCl |
| D、久置后的氯水酸性变弱 |
今年全国低碳日活动的主题是:“携手节能低碳、共建碧水蓝天”.下列措施与这主题不相符的是( )
A、 焚烧废弃塑料 |
B、 处理污水 |
C、 风力发电 |
D、 推广电动汽车 |