题目内容
7. 在恒容密闭容器中加入一定量的反应物后存在下列平:CO(g)+H2O(g)?CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示,下列说法正确的是( )
在恒容密闭容器中加入一定量的反应物后存在下列平:CO(g)+H2O(g)?CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示,下列说法正确的是( )| A. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| B. | 在T2时,若反应处于状态D,则一定有ν正<ν逆 | |
| C. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1>K2 |
分析 A.由图可知,温度越高平衡时c(CO2)越大,说明升高温度平衡向正反应移动;
B.T2时反应进行到状态D,c(CO2)高于平衡浓度,故反应向逆反应进行;
C.A、C点温度不同,升高温度平衡正向移动,CO的浓度减小;
D.化学平衡常数只受温度影响,升高温度平衡向吸热反应移动,根据平衡移动判断温度对平衡常数的影响.
解答 解:A.由图可知,温度越高平衡时c(CO2)越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应进行,故正反应是吸热反应,即△H>0,故A正确;
B.T2时反应进行到状态D,c(CO2)高于平衡浓度,故反应向逆反应进行,则一定有ν正<ν逆,故B正确;
C.平衡状态A与C相比,C点温度高,已知△H>0,升高温度平衡正移,CO浓度减小,所以A点CO浓度大,故C错误;
D.该反应正反应是吸热反应,升高温度平衡向正反应移动,化学平衡常数增大,故K1<K2,故D错误;
故选AB.
点评 本题考查化学平衡,为高频考点,把握图中温度对浓度的影响、K与温度的关系、平衡移动为解答的关键,侧重分析与应用能力的考查,注意图象的分析与应用,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
9.下列说法正确的是( )
| A. | 干冰升华时要吸收热量,所以这是吸热反应 | |
| B. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| C. | 浓硫酸具有强氧化性,常温下不可用铝罐盛装 | |
| D. | 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 |
18.下列叙述正确的是( )
| A. | 加热能够抑制水的电离 | |
| B. | 金属发生吸氧腐蚀时,被腐蚀的速率和氧气浓度无关 | |
| C. | 原电池中发生的反应达到平衡时,该电池仍有电流产生 | |
| D. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
2.下列各组液体混合物能用分液漏斗分离的是( )
| A. | 乙酸和水 | B. | 乙醇和水 | C. | 乙醇和乙酸 | D. | 苯和水 |
12.下列说法或表示方法正确的是( )
| A. | 氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| B. | 等质量的硫蒸气和硫磺分别完全燃烧,二者放出的热量一样多 | |
| C. | 已知中和热为57.3 kJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-Q1 kJ/mol 2H2(g)+O2(g)═2H2O(g)△H=-Q2 kJ/mol,则Q1>Q2 |
19.图中,R、W、X、Y、Z为元素周期表中前四周期的部分元素,下列有关叙述正确的是( )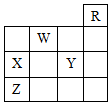

| A. | 五种元素中,只有Z为金属元素 | |
| B. | W位于ⅥA族,有+6、-2两种常见化合价 | |
| C. | X和Y的最高价氧化物对应水化物都是强酸 | |
| D. | X、Y、Z的气态氢化物的稳定性:Y>X>Z |
16.设NA为阿伏加德罗常数的数值.下列有关叙述不正确的是( )
| A. | 44 g乙醛中所含的氧原子数为NA | |
| B. | 常温常压下,8gCH4含有5 NA个电子 | |
| C. | 标准状况下,22.4L苯含有NA个C6H6分子 | |
| D. | 14 g乙烯中所含的C-H键数目为2NA |
10.下列有关铝及其化合物的说法正确的是( )
| A. | 可用NaOH溶液除去Fe2O3中的Al2O3 | |
| B. | 铝表面有氧化膜保护,铝锅可以长时间盛放酸性溶液 | |
| C. | 氯化铝溶液与NaOH溶液互滴现象完全相同 | |
| D. | 实验室常用NaOH溶液和AlCl3溶液制备Al(OH)3 |