题目内容
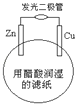
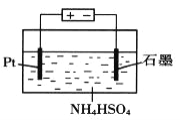
【题目】O3是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是

A. 电极a为阴极
B. a极的电极反应为O2+4H++4e-===2H2O
C. 电解一段时间后b极周围的pH下降
D. 标准状况下,当有5.6LO2反应时,收集到O2和O3混合气体4.48L,O3的体积分数为80%
【答案】D
【解析】
本题结合电解池的新型应用,主要考查电解池相关知识。电解池左侧通入O2,由此可知,a极发生还原反应,a极为阴极,其电极反应式为:O2+4H++4e-=2H2O,故b为阳极,由此进行分析即可。
A.由上述分析可知,a为阴极,正确;
B.由上述分析可知,a极的电极反应为O2+4H++4e-=2H2O,正确;
C.b极为H2O电离出的OH-失去电子,生成O2和O3,电解一段时间后,b极附近水的电离平衡被破坏,溶液中H+浓度增大,pH下降,正确;
D.阴极0.25molO2反应时,转移电子为1mol,即阳极消耗0.5molH2O,生成混合气体为0.2mol,设生成O2为mmol,O3为nmol,由此可列出二元一次方程组:2m+3n=0.5,m+n=0.2,解得n=0.1,m=0.1,故O3的体积分数为![]() ,错误。答案选D。
,错误。答案选D。

练习册系列答案
相关题目
【题目】下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性.Cl2>Br2>I2 |
C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
D | 浓HNO3加热 | 有红棕色气体 | HNO3有强氧化性 |
A. A B. B C. C D. D