题目内容
下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.盖斯定律,可计算某些难以直接测量的反应的焓变 |
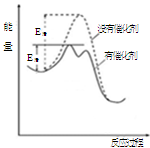
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |
C
试题分析:A、生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,故A错误;B、反应速率与反应是吸热还是放热无关,反应速率与反应物本身的性质及外界条件有关,故B错误;C、反应的热效应只与始态、终态有关,与过程无关,根据盖斯定律可计算某些难以直接测量的反应焓变,故C正确;D、反应的热效应只与始态、终态有关,与过程无关,所以同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同,故D错误,答案选C。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
 2SO3;ΔH =-196.6kJ/mol
2SO3;ΔH =-196.6kJ/mol