题目内容
下图中表示A~G七种物质的转化关系。若将A、B、C、D、G分别灼烧,火焰都呈黄色;A单质能跟水起剧烈反应生成C,B为淡黄色固体,F常温下为液态。请回答:
(1)B为 ;C为 ;D为 ;(写化学式)
(2)将适量B和滴有酚酞的水反应,实验现象为 ;
(3)G受热分解生成D、E、F,化学方程式为 ;
(4)将C的溶液与Al(OH)3混合,可看到固体逐渐溶解,反应的离子方程式为
。
(1)B为 Na2O2 ;C为 NaOH ;D为 Na2CO3 ;
(2)有大量气泡产生,气体使带火星的木条复燃,试管外壁发热,溶液颜色先变红后褪色 ;
(3) 2NaHCO3![]() Na2CO3+CO2↑+H2O ;
Na2CO3+CO2↑+H2O ;
(4) Al(OH)3+OH-=AlO2-+2H2O 。

练习册系列答案
相关题目



 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).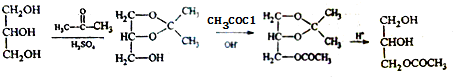








 (用反应流程图表示,并注明反应条件)。
(用反应流程图表示,并注明反应条件)。