题目内容
3.下列说法正确的是( )| A. | NaHCO3+H2$?_{释氢}^{储氢}$HCOONa+H20反应中,储氢、释氢过程均无能量变化 | |
| B. | 2NO(g)+2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 | |
| C. | 化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律 | |
| D. | 2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的△H相等 |
分析 A.储氢释氢是化学变化,化学变化中一定伴随能量变化;
B.正反应为熵减的反应,根据△H-T△S=△G<0反应自发进行进行判断;
C.化学变化产生了新物质.化学变化是原子的重新分配与组合,反应前后原子的种类、原子的数目、原子的质量都没有改变,因而质量守恒,遵循质量守恒定律;化学变化是旧的化学键断裂,新的化学键形成的过程,化学键断裂要吸收能量,化学键形成要放出能量,遵循能量守恒定律;
D.焓变与化学计量数及各物质的状态有关.
解答 解:A.储氢、释氢过程都是化学变化,化学变化中一定伴随能量变化,故A错误;
B.正反应为熵减的反应,即△S<0,常温下能自发进行,则△H-T△S=△G<0,则该反应的焓变△H<0,故B错误;
C.化学变化发生的是质变,产生了新物质;化学变化是原子的重新分配与组合,从原子水平而言,反应前后原子的种类、原子的数目、原子的质量都没有改变,因而质量守恒,遵循质量守恒定律.因为化学变化是旧的化学键断裂,新的化学键形成的过程,化学键断裂要吸收能量,化学键形成要放出能量,遵循能量守恒定律,故C正确;
D.反应2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的化学计量数不同,则二者的△H不同,故D错误;
故选C.
点评 本题考查了反应热与焓变,题目难度中等,明确化学反应与能量变化的关系为解答关键,注意掌握判断反应能否自发进行的方法,试题充分考查学生的分析能力及灵活应用能力.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
14.在一个10L的密闭容器中,发生反应H2(g)+I2(g)?2HI(g),起始加入H2的物质的量为2mol,I2的物质的量为5mol,5s后,HI的物质的量为0.5mol,则这5s内H2的反应速率为( )
| A. | 0.04mol•L-1•s-1 | B. | 0.005mol•L-1•s-1 | ||
| C. | 0.01mol•L-1•s-1 | D. | 0.1mol•L-1•s-1 |
18.NA代表阿伏伽德罗常数,下列说法不正确的是( )
| A. | 1mol Ne含有的电子数目为10NA | |
| B. | 0.2NA个硫酸分子与19.6g磷酸含有相同的氧原子数 | |
| C. | 2.8g氮气所含的分子数为NA | |
| D. | 1.8gNH4+中含有的质子数为NA |
4.下列有关实验装置的说法中正确的是( )
| A. |  除去氯气中的氯化氢 | B. |  向容量瓶中转移溶液 | ||
| C. | 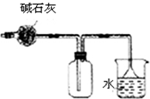 干燥并收集氨气 | D. |  保存浓硝酸 |

 ,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.