题目内容
酸碱中和滴定在生产实际中有着广泛的应用。室温时,用0.250 mol/LNaOH溶液滴定25.0 mL的一元酸HR溶液时,溶液的pH变化情况如图所示,其中a点表示两种物质恰好完全反应。请回答下列问题:
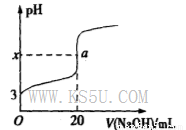
(1)该一元酸HR溶液的物质的量浓度为_______________。
(2)图中x_____7(填“>”、“<”或“=”),其原因是___________________(用离子方程式表示)。
(3)滴定到a点时,溶液中c(OH-)--c(HR)=____mol/L (用含x的代数式表示)。
(4)室温时,HR的电离常数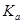 =____________mol/L。
=____________mol/L。
(1)0.20mol/L (2)> R-+H2O  HR+OH-
(3)10-x
(4)5.0×10-6
HR+OH-
(3)10-x
(4)5.0×10-6
【解析】
试题分析:(1)由于酸碱恰好发生中和反应时:n(NaOH)=n(HR),所以20ml×0.250
mol/L=25.0 mL×C(HR) mol/L,解得C(HR)= 0.20mol/L.(2)反应开始时C(H+)=10-3mol/L<C(HR) =0.20mol/L,说明HR为弱酸。二者恰好反应时生成的盐为强碱弱酸盐,在溶液中发生反应:R-+H2O  HR+OH-,所以图中X>7,,溶液显碱性。(3)恰好中和时PH=X。C(H+)=10-Xmol/L,则C(OH-)(总)=KW÷C(H+)=10-14÷10-X=10(X-14)
HR+OH-,所以图中X>7,,溶液显碱性。(3)恰好中和时PH=X。C(H+)=10-Xmol/L,则C(OH-)(总)=KW÷C(H+)=10-14÷10-X=10(X-14)
C(OH-)(总)=C(OH-)(水电离)+C(OH-)(水解)=C(H+)+C(HR),所以C(OH-)(总) --C(HR) =C(H+)=10-Xmol/L。
(4)室温时,在溶液中存在电离平衡HR H++R-,电离常数Ka={C(H+)·C(R-)}÷C(HR)={10-3
mol/L×10-3 mol/L}÷{0.20mol/L-10-3
mol/L }=5.0×10-6 mol/L。
H++R-,电离常数Ka={C(H+)·C(R-)}÷C(HR)={10-3
mol/L×10-3 mol/L}÷{0.20mol/L-10-3
mol/L }=5.0×10-6 mol/L。
考点:考查酸碱中和滴定及强碱弱酸盐溶液中离子浓度的大小比较、弱酸的电离平衡常数等知识。

| A、实验中所用到的滴定管、容量瓶,在使用前均需要检漏 | B、如果实验中需用60mL的稀硫酸标准溶液,配制时应选用100mL容量瓶 | C、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大 | D、用甲基橙作指示剂,滴定终点时,溶液颜色从橙色变为红色 |