题目内容
下表为元素周期表前四周期的一部分,下列有关X、W、Y、R、Z五种元素的叙述中正确的是( )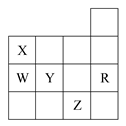
| A.常温常压下,五种元素的单质中有两种是气态 |
| B.Y、Z的阴离子的电子层结构都与R原子的相同 |
| C.X的氢化物与其最高价氧化物对应的水化物形成的盐溶液呈碱性 |
| D.Y元素最高价氧化物对应的水化物的酸性比W元素的弱 |
A
解析

练习册系列答案
相关题目
下列各组原子中,彼此化学性质一定相似的是
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C.2p轨道上有三个未成对电子的X原子与3p轨道上有三个未成对电子的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
(2012北京理综,9)已知33As、35Br位于同一周期。下列关系正确的是( )。
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
下列有关表述正确的是( )
| A.硫离子的电子排布式:1s22s22p63s23p4 |
B.H2O的电子式: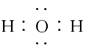 |
C.N原子最外层电子的轨道表示式: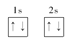 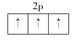 |
D.K的原子结构示意图: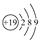 |
A和B是短周期元素,A2-与B+的核外电子总数之差为8,则下列说法正确的是( )
| A.A和B的原子序数之差为8 |
| B.A和B原子的最外层电子数之和为8 |
| C.A和B原子的最外层电子数之差为7 |
| D.A和B原子的核外电子数总和可能为11 |
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是( )
| A.X与W形成的化合物W2X2中含有离子键和共价键 |
| B.原子半径大小的顺序为W>X>Y>Z |
| C.Y、Z两元素形成的简单阴离子的还原性Z>Y |
| D.Y、Z两元素最高价氧化物对应水化物的酸性Z>Y |
元素周期表和元素周期律对化学学习具有指导意义,下列有关叙述正确的是( )
| A.铅位于周期表中金属与非金属元素交界处,可做半导体材料 |
| B.若存在简单阴离子R2-,则R一定属于第ⅥA族元素 |
| C.S和Se属于第ⅥA族元素,H2S还原性比H2Se的强 |
| D.元素原子最外层电子数较少的金属一定比最外层电子数较多的金属活动性强 |
某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是 ( )。
| A.电子排布式为1s22s22p63s23p63d34s2 |
| B.该元素为V |
| C.该元素为ⅡA族元素 |
| D.该元素位于d区 |