题目内容
【题目】将铁、铝的混合物加入到足量氢氧化钠溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的硫酸铜溶液中,充分反应后过滤得到的固体质量正好与原固体质量相等,则原固体中铝的质量分数为( )
A. 14.3% B. 12.5% C. 87.5% D. 无法计算
【答案】B
【解析】
将铁、铝的混合物加入到足量的NaOH溶液中,反应后剩余固体为Fe,再将过滤得到的固体Fe加入到足量的CuSO4溶液中,会置换出Cu,充分反应后过滤得到的固体Cu的质量恰好与原固体质量相等,说明反应Fe+CuSO4═FeSO4+Cu中Fe完全时固体质量增重等于原混合物中Al的质量,假设固体增重为8g,结合差量法计算混合物中铁的质量,然后计算出铝的质量分数。
得到的固体Cu的质量恰好与原固体质量相等,说明反应Fe+CuSO4═FeSO4+Cu中Fe完全反应时固体质量增重等于原混合物中Al的质量,假设固体增重为8g,则混合物中Al的质量也是8g,
设混合物中Fe的质量为x,则:
Fe+CuSO4═FeSO4+Cu 质量增重
56 6456=8
x 8g
故x = 8g×56/8 = 56 g
则混合物中Al的质量分数为![]() ×100% = 12.5%
×100% = 12.5%
答案选B。

【题目】N-苯基苯甲酰胺 广泛应用于药物,可由苯甲酸
广泛应用于药物,可由苯甲酸 与苯胺
与苯胺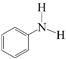 反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤-重结晶等,最终得到精制的成品。
反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤-重结晶等,最终得到精制的成品。
已知:
溶剂 物质 | 水 | 乙醇 | 乙醚 |
苯甲酸 | 微溶 | 易溶 | 易溶 |
苯胺 | 易溶 | 易溶 | 易溶 |
N-苯基苯甲酰胺 | 不溶 | 易溶于热乙醇,冷却后易于结晶析出 | 微溶 |
下列说法不正确的是
A. 反应时断键位置为C-O键和N-H键
B. 洗涤粗产品用水比用乙醚效果更好
C. 产物可选用乙醇作为溶剂进行重结晶提纯
D. 硅胶吸水,能使反应进行更完全