题目内容
12.下列离子方程式正确的是( )| A. | 钢铁发生吸氧或析氢腐蚀时,铁均作负极被氧化:Fe-3e-=Fe3+ | |
| B. | SO2气体通入Fe2(SO4)3溶液中:SO2+2H2O+2Fe3+=2Fe2++4H++SO42- | |
| C. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$ 2Cu+O2↑+4H+ | |
| D. | 明矾溶液中滴加Ba(OH)2溶液至SO42-完全沉淀:Al3++Ba2++SO42-+3OH-═BaSO4↓+Al(OH)3↓ |
分析 A.铁发生腐蚀时失去2个电子生成亚铁离子;
B.铁离子具有氧化性,能够将二氧化硫氧化成硫酸根离子;
C.铜为电极,相当于电解精炼铜,阳极铜失去电子,不会生成氧气;
D.硫酸根离子完全沉淀时,铝离子与氢氧根离子的物质的量之比为1:4,反应生成偏铝酸根离子.
解答 解:A.钢铁发生吸氧或析氢腐蚀时,铁均作负极失去2个电子生成亚铁离子,正确的电极反应式为:Fe-2e-=Fe2+,故A错误;
B.SO2气体通入Fe2(SO4)3溶液中,二者发生氧化还原反应,反应的离子方程式为:SO2+2H2O+2Fe3+=2Fe2++4H++SO42-,故B正确;
C.用铜做电极电解CuSO4溶液,阳极金属铜失去电子,不会生成氧气,故C错误;
D.明矾溶液中滴加Ba(OH)2至SO42-完全沉淀,铝离子恰好反应生成偏铝酸根离子,反应的化学方程式为:KAl(SO4)2+2Ba(OH)2=2BaSO4↓+KAlO2+2H2O,对应的离子方程为:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等,C为易错点,注意电极为铜,阳极铜失去电子.

练习册系列答案
相关题目
2.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1molFe与1molCl2充分反应,转移的电子数为3NA | |
| B. | NA个Fe(OH)3胶体粒子形成的纳米材料的质量为107g | |
| C. | 含有4.6g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| D. | 标准状况下,22.4 LSO3含有NA个分子 |
20.下列反应的离子方程式书写正确的是( )
| A. | 石灰乳与稀盐酸反应:OH-+H+═H2O | |
| B. | 用稀硫酸除去铜绿:4H++Cu2(OH)2CO3═2Cu2++CO2↑+3H2O | |
| C. | NaHCO3溶液中滴加过量的Ba(OH)2溶液:2HCO3-+2OH-+Ba2+═BaCO3↓+CO32-+2H2O | |
| D. | 等体积、等浓度的Ca(HCO3)2溶液与NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
7.下列有关化学用语表达正确的是( )
| A. | H2O2的电子式: | |
| B. | 二氧化硅的分子式:SiO2 | |
| C. | 乙酸分子的球棍模型: | |
| D. | 离子结构示意图 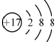 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- |
4.标准状况下,一个钢瓶若装满O2时质量为 79g,若装满氮气时的质量是71g,若装满某气体X时质量为103g,下列说法错误的是( )
| A. | 此钢瓶的容积为44.8L | |
| B. | 此钢瓶的质量为15g | |
| C. | 气体X对氢气的相对密度为22 | |
| D. | 该状况下此钢瓶中盛满氯气时的总质量为142g |
10.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法的是( )
| A. | 将混合气体通过盛有酸性KMnO4溶液的洗气瓶 | |
| B. | 将混合气体通过盛有适量溴水的洗气瓶 | |
| C. | 将混合气体中通入氢气,在Ni催化加热的条件下反应 | |
| D. | 将混合气体通过盛有NaOH溶液的洗气瓶 |

