题目内容
【题目】某实验小组同学进行如下实验,以检验化学反应中的能量变化. 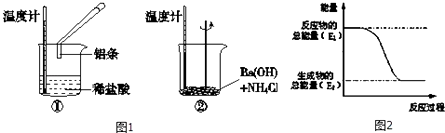
请回答下列问题:
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是热反应,Ba(OH)28H2O与NH4Cl的反应是热反应.反应过程(填“①”或“②”)的能量变化可用图2表示.
(2)下列变化属于放热反应的是 A.碳酸钙的分解反应 B.酸碱中和反应 C.碳和水蒸气的反应 D.浓硫酸稀释 E.实验室制取氨气 F.实验室制取氢气
(3)现有如下两个反应:(A)NaOH+HCl═NaCl+H2O (B)2FeCl3+Cu═2FeCl2+CuCl2①以上两个反应能设计成原电池的是
②写出设计原电池正、负极电极反应式正极:负极: .
【答案】
(1)放;吸;①
(2)B、F
(3)B;2Fe3++2e﹣=2Fe2+;Cu﹣2e﹣=Cu2+
【解析】解:(1)Al与HCl反应后,温度升高,则说明反应放热,Ba(OH)28H2O与NH4Cl的反应温度降低,说明反应为吸热反应;反应①为放热反应,反应物的总能量大于生成物的总能量,所以①的能量变化可用图2表示;所以答案是:放;吸;①;(2)酸碱中和、活泼金属与酸的反应为放热反应,BF为放热反应,ACE为吸热反应,D不是化学反应,所以答案是:BF;(3)①自发进行的放热的氧化还原反应能设计成原电池,A反应中没有电子转移,不属于氧化还原反应,所以不能设计成原电池;B属于自发进行的放热的氧化还原反应,所以能设计成原电池,所以答案是:B;②该原电池中,Cu失电子作负极,不如Cu活泼的金属或导电的非金属性作正极,电解质溶液为可溶性的氯化铁溶液,正极上铜离子得电子发生还原反应,电极反应式为:2Fe3++2e﹣=2Fe2+ , 负极上Cu失电子发生氧化反应,电极反应式为:Cu﹣2e﹣═Cu2+;所以答案是:2Fe3++2e﹣=2Fe2+;Cu﹣2e﹣=Cu2+ .
【考点精析】根据题目的已知条件,利用吸热反应和放热反应的相关知识可以得到问题的答案,需要掌握化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的物质化学式为 .
(3)①③⑦中形成的简单离子半径由大到小的顺序是 .
(4)元素⑦的氢化物分子式为 , 用电子式表示该物质的形成过程 .
(5)⑧的最高价氧化物对应的水化物化学式为 . ①和⑨两元素形成化合物的化学式为 , 该化合物灼烧时焰色为 , 该化合物的溶液与元素⑧的单质反应的离子方程式为 .