题目内容
【化学与生活】
2010年第41届世博会在上海成功举办,其主题是“城市,让生活更美好”.
(1)低碳经济是以低能耗、低污染、低排放为基础的经济模式,上海世博会的亮点之一是实现“二氧化碳零排放”.
①世博停车场,安装有汽车尾气催化光解设施,它能将汽车尾气中CO和NOx反应生成可参与大气生态环境循环的无毒气体,写出CO和NO在一定条件下反应的化学方程式: .
②使用传统催化剂,使二氧化碳与某些有机物反应可以生成塑料,但反应时间长.目前诞生的纳米级催化剂增加了催化剂的表面积,提高了 (选填“反应速率”、“产品质量”或“原料利用率”).使用这种塑料能减少白色污染,因为它在微生物作用下,可以实现100%的降解.
③合理利用二氧化碳,可以提高生活质量,促进工业发展.在常压下,-78℃时,二氧化碳气体凝结成固态二氧化碳,俗称干冰.某学生买回一盒冰淇淋月饼,盒里有很多作为致冷剂的碎干冰.下列关于干冰处理的正确做法是
(A)将干冰放入冰箱 (B)让干冰在通风处自然升华
(C)直接将干冰倒入下水道 (D)用手取干冰扔入废物箱
④现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为 ;人们已尝试使用 作为汽车燃料可真正实现“二氧化碳零排放”.
(2)上海世博为实现环保世博、生态世博目标,如日本馆的超轻“膜结构”,能发电,会呼吸;澳大利亚馆外表,覆盖着比不锈钢更便宜耐用的“耐候钢”.因此材料是人类赖以生存和发展的重要物质基础.
①2010年上海世博会中国馆“东方之冠”的主体结构是用国产Q460钢制成的. 下列有关Q460钢的性质中,属于化学性质的是
A.强度高 B.能导电 C.耐腐蚀 D.抗震性好
②耐候钢看起来有些锈迹斑斑,再仔细一瞧却是光滑如新,这得益于耐候钢在大气中具有优良的抗蚀性能.请你列举两种防止铁制品被腐蚀的方法 、 .
③石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是 (填化学式);有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种 (选填“橡胶”或“纤维”或“塑料”).
④日本馆的超轻“膜结构”,这层膜白天能透过阳光,利用太阳能发电,从而实现了将 转化为 .
2010年第41届世博会在上海成功举办,其主题是“城市,让生活更美好”.
(1)低碳经济是以低能耗、低污染、低排放为基础的经济模式,上海世博会的亮点之一是实现“二氧化碳零排放”.
①世博停车场,安装有汽车尾气催化光解设施,它能将汽车尾气中CO和NOx反应生成可参与大气生态环境循环的无毒气体,写出CO和NO在一定条件下反应的化学方程式:
②使用传统催化剂,使二氧化碳与某些有机物反应可以生成塑料,但反应时间长.目前诞生的纳米级催化剂增加了催化剂的表面积,提高了
③合理利用二氧化碳,可以提高生活质量,促进工业发展.在常压下,-78℃时,二氧化碳气体凝结成固态二氧化碳,俗称干冰.某学生买回一盒冰淇淋月饼,盒里有很多作为致冷剂的碎干冰.下列关于干冰处理的正确做法是
(A)将干冰放入冰箱 (B)让干冰在通风处自然升华
(C)直接将干冰倒入下水道 (D)用手取干冰扔入废物箱
④现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为
(2)上海世博为实现环保世博、生态世博目标,如日本馆的超轻“膜结构”,能发电,会呼吸;澳大利亚馆外表,覆盖着比不锈钢更便宜耐用的“耐候钢”.因此材料是人类赖以生存和发展的重要物质基础.
①2010年上海世博会中国馆“东方之冠”的主体结构是用国产Q460钢制成的. 下列有关Q460钢的性质中,属于化学性质的是
A.强度高 B.能导电 C.耐腐蚀 D.抗震性好
②耐候钢看起来有些锈迹斑斑,再仔细一瞧却是光滑如新,这得益于耐候钢在大气中具有优良的抗蚀性能.请你列举两种防止铁制品被腐蚀的方法
③石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是
④日本馆的超轻“膜结构”,这层膜白天能透过阳光,利用太阳能发电,从而实现了将
分析:(1)①CO和NO在一定条件下反应生成氮气和二氧化碳;
②催化剂加快反应速率;
③干冰易升华;
④物质的量相同的乙醇(C2H5OH)与汽油(设为C8H18),由C原子守恒可知生成的二氧化碳的物质的量之比为2:8;
(2)①耐腐蚀为物质不易反应的性质,为化学性质;
②防止铁制品被腐蚀,可加保护层或利用电化学原理保护;
③石英玻璃中主要含SiO2,有机玻璃(聚甲基丙烯酸甲酯)为有机高分子材料;
④利用太阳能发电,实现太能能转化为电能.
②催化剂加快反应速率;
③干冰易升华;
④物质的量相同的乙醇(C2H5OH)与汽油(设为C8H18),由C原子守恒可知生成的二氧化碳的物质的量之比为2:8;
(2)①耐腐蚀为物质不易反应的性质,为化学性质;
②防止铁制品被腐蚀,可加保护层或利用电化学原理保护;
③石英玻璃中主要含SiO2,有机玻璃(聚甲基丙烯酸甲酯)为有机高分子材料;
④利用太阳能发电,实现太能能转化为电能.
解答:解:(1)①CO和NO在一定条件下反应生成氮气和二氧化碳,该反应为2CO+2NO
N2+2CO2,故答案为:2CO+2NO
N2+2CO2;
②目前诞生的纳米级催化剂增加了催化剂的表面积,提高了反应速率,故答案为:反应速率;
③干冰易升华,让干冰在通风处自然升华的做法最合适,其它选项不可取,故答案为:B;
④物质的量相同的乙醇(C2H5OH)与汽油(设为C8H18),由C原子守恒可知生成的二氧化碳的物质的量之比为2:8=1:4,产生二氧化碳会加剧温室效应,则尝试使用氢气作为汽车燃料可真正实现“二氧化碳零排放”,故答案为:1:4;氢气;
(2)①耐腐蚀为物质不易反应的性质,为化学性质,而强度、导电、抗震性均为物理性质,故答案为:C;
②防止铁制品被腐蚀的方法有在铁器表面生成一层致密的氧化膜、刷油漆、电镀、外加电流阴极保护法等,故答案为:刷油漆;电镀;
③石英玻璃中主要含SiO2,有机玻璃(聚甲基丙烯酸甲酯)为有机高分子材料,属于速率,故答案为:SiO2;塑料;
④利用太阳能发电,实现太能能转化为电能,故答案为:太阳能;电能.
| ||
| ||
②目前诞生的纳米级催化剂增加了催化剂的表面积,提高了反应速率,故答案为:反应速率;
③干冰易升华,让干冰在通风处自然升华的做法最合适,其它选项不可取,故答案为:B;
④物质的量相同的乙醇(C2H5OH)与汽油(设为C8H18),由C原子守恒可知生成的二氧化碳的物质的量之比为2:8=1:4,产生二氧化碳会加剧温室效应,则尝试使用氢气作为汽车燃料可真正实现“二氧化碳零排放”,故答案为:1:4;氢气;
(2)①耐腐蚀为物质不易反应的性质,为化学性质,而强度、导电、抗震性均为物理性质,故答案为:C;
②防止铁制品被腐蚀的方法有在铁器表面生成一层致密的氧化膜、刷油漆、电镀、外加电流阴极保护法等,故答案为:刷油漆;电镀;
③石英玻璃中主要含SiO2,有机玻璃(聚甲基丙烯酸甲酯)为有机高分子材料,属于速率,故答案为:SiO2;塑料;
④利用太阳能发电,实现太能能转化为电能,故答案为:太阳能;电能.
点评:本题考查常见的生活环境的污染及治理,把握汽车尾气、环境污染的处理、能源利用及能量转化、材料及电化学原理为解答的关键,注重化学与生活、环境保护的联系,综合性较强,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目




 同分异构体的结构简式:
同分异构体的结构简式:




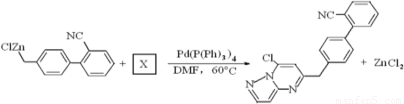
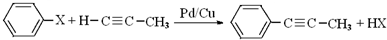
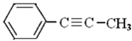 同分异构体的结构简式:
同分异构体的结构简式: