题目内容
下列说法不正确的是( )
| A、同主族元素的单质及化合物的化学性质发生递变是由其电子层数的递变引起的 |
| B、过渡元素包括了大部分金属元素 |
| C、第4、5、6周期称为长周期 |
| D、第7周期若填满,可有50种元素 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A.同主族元素,最外层电子数相同,而电子层数不同;
B.过渡元素均为金属元素;
C.7个周期中,1、2、3周期为短周期,其余为长周期;
D.第7周期若填满,与第6周期元素的种类数相同.
B.过渡元素均为金属元素;
C.7个周期中,1、2、3周期为短周期,其余为长周期;
D.第7周期若填满,与第6周期元素的种类数相同.
解答:
解:A.同主族元素,最外层电子数相同,而电子层数不同,则同主族元素的单质及化合物的化学性质发生递变是由其电子层数的递变引起的,故A正确;
B.过渡元素均为金属元素,目前80多种金属元素在主族的为22种,即过渡元素包括了大部分金属元素,故B正确;
C.7个周期中,1、2、3周期为短周期,其余为长周期,则第4、5、6周期称为长周期,故C正确;
D.第7周期若填满,与第6周期元素的种类数相同,应有32种元素,故D错误;
故选D.
B.过渡元素均为金属元素,目前80多种金属元素在主族的为22种,即过渡元素包括了大部分金属元素,故B正确;
C.7个周期中,1、2、3周期为短周期,其余为长周期,则第4、5、6周期称为长周期,故C正确;
D.第7周期若填满,与第6周期元素的种类数相同,应有32种元素,故D错误;
故选D.
点评:本题考查元素周期表的结构及应用,为高频考点,把握周期表的结构及元素的位置、周期中元素的种类数为解答的关键,侧重分析能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NA表示阿伏加德罗常数,以下各物质所含分子数最多的是( )
| A、标准状况下11.2L氯气 |
| B、含2NA个氢分子的氢气 |
| C、0.8mol氧气 |
| D、17g氨气(NH3的摩尔质量为17g?mol-1) |
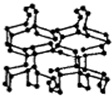 在高压下氮气会聚合生成高聚氮,这种高聚氮的晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构(如图).已知晶体中N-N键的键能为160kJ?mol-1,而N≡N的键能为942kJ?mol-1.则下列有关说法正确的是( )
在高压下氮气会聚合生成高聚氮,这种高聚氮的晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构(如图).已知晶体中N-N键的键能为160kJ?mol-1,而N≡N的键能为942kJ?mol-1.则下列有关说法正确的是( )| A、高聚氮与氮气互为同位素 |
| B、14g高聚氮含3.01×1023个氮原子 |
| C、高聚氮中氮原子为非极性键 |
| D、高聚氮转变成氮气是氧化还原反应 |
常温下,将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,溶液中c(H+)最接近于( )
| A、(10-8+10-10)mol/L | ||
| B、(10-4+10-6)mol/L | ||
C、
| ||
| D、2×10-10mol/L |
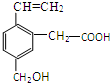 某有机物的结构为如图所示,这种有机物不可能具有的性质是( )
某有机物的结构为如图所示,这种有机物不可能具有的性质是( )①能使酸性KMnO4溶液褪色;
②能跟NaOH溶液反应;③能发生酯化反应;
④能发生加成反应;⑤能发生水解反应.
| A、①④ | B、①⑤ | C、只有⑤ | D、④ |
要制得较纯净的溴乙烷,最好的方法是( )
| A、乙烷与溴发生取代反应 |
| B、乙烯与溴化氢发生加成反应 |
| C、乙烯与溴发生加成反应 |
| D、乙炔与溴化氢发生加成反应 |
S2Cl2是广泛用于橡胶工业的硫化剂,常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,其结构与H2O2类似.下列说法错误的是( )
| A、S2Cl2分子中的两个S原子均是sp3杂化 |
| B、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
| C、S2Br2与S2Cl2结构相似,熔沸点S2Br2>S2Cl2 |
| D、S2Cl2分子中的S为-1价,既含有极性键又含有非极性键 |
实验室里进行过滤、蒸发和配制物质的量浓度的操作时,都要用到的仪器是( )
| A、烧杯 | B、玻璃棒 |
| C、蒸发皿 | D、酒精灯 |