题目内容
NA表示阿伏加德罗常数,以下各物质所含分子数最多的是( )
| A、标准状况下11.2L氯气 |
| B、含2NA个氢分子的氢气 |
| C、0.8mol氧气 |
| D、17g氨气(NH3的摩尔质量为17g?mol-1) |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据N=nNA可知,分子数与物质的量成正比,物质所含分子数最多,说明该物质的物质的量最大;先将各选项中的量转化成物质的量,然后进行比较即可.
解答:
解:A.标准状况下11.2 L氯气的物质的量为0.5mol;
B.含2NA个氢分子的氢气,其物质的量为:
mol=2mol;
C.0.8mol氧气;
D.17g氨气的物质的量为:
=1mol;
根据以上分析可知,物质的量最大的是B,根据N=nNA可知,含有分子数最多的是B,
故选B.
B.含2NA个氢分子的氢气,其物质的量为:
| 2NA |
| NA |
C.0.8mol氧气;
D.17g氨气的物质的量为:
| 17g |
| 17g/mol |
根据以上分析可知,物质的量最大的是B,根据N=nNA可知,含有分子数最多的是B,
故选B.
点评:本题考查阿伏加德罗常数的有关计算,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确物质的量与物质分子数成正比为解答本题的关键.

练习册系列答案
相关题目
已知A、B是第一周期以外的短周期元素,它们可以形成离子化合物AmBn.在此化合物中,所有离子均能形成稀有气体原子的稳定结构.若A的核电荷数为a,则B的核电荷数不可能是( )
| A、a+8-m-n |
| B、a+18-m-n |
| C、a+16-m-n |
| D、a-m-n |
地壳中含量第一和第二的两元素形成的化合物,不具有的性质( )
| A、熔点很高 |
| B、能与水反应生成对应的酸 |
| C、可与纯碱反应 |
| D、与碳在高温下反应可制取两元素中的一种单质 |
下列说法错误的是( )
| A、0.1mol某醛与足量的银氨溶液反应,产生银的质量为21.6g,则该醛肯定为二元醛 |
| B、乙醇、苯酚、乙酸都有羟基,但是电离常数不同,这主要是基团之间相互影响造成的 |
C、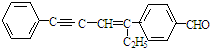 分子中最多19个碳原子共平面、最多6个原子共直线 分子中最多19个碳原子共平面、最多6个原子共直线 |
| D、分子式为C10H20O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C,则有机物A的可能结构有4种 |
已知下列两个结构简式:CH3-CH3和CH3-,两式中均有短线“-”,这两条短线所表示的意义是( )
| A、都表示一对共用电子对 |
| B、都表示一个共价单键 |
| C、前者表示一对共用电子对,后者表示一个未成对电子 |
| D、前者表示分子内只有一个共价单键,后者表示该基团内无共价单键 |
下列与生活相关的叙述错误的是( )
| A、酸性臭氧水(AOW)可用于消灭HlNl病毒,因为臭氧具有强氧化性 |
| B、水的处理常用到漂白粉和明矾,二者的作用原理相同 |
| C、二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成 |
| D、三聚氰胺添入牛奶中能增加含氮量,但有害健康 |
下列物质均具有漂白作用,其中一种与另外三种的漂白原理不同的是( )
| A、HClO |
| B、H2O2 |
| C、SO2 |
| D、O3 |
NA为阿伏加德罗常数,下列物质所含分子数最少的是( )
| A、3.6g水(水的摩尔质量为18g?mol-1) |
| B、含NA个氢分子的氢气 |
| C、0.8mol氧气 |
| D、标准状况下2.24L氨气 |
下列说法不正确的是( )
| A、同主族元素的单质及化合物的化学性质发生递变是由其电子层数的递变引起的 |
| B、过渡元素包括了大部分金属元素 |
| C、第4、5、6周期称为长周期 |
| D、第7周期若填满,可有50种元素 |