题目内容
将Na2CO3?10H2O与NaHCO3的混合物m g溶解于水,配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,若将溶液蒸干并加热至质量不变,可得固体的质量是( )A.1.86g
B.2.55g
C.2.12g
D.无法确定
【答案】分析:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,最后得到的固体为Na2CO3,根据Na元素守恒可计算Na2CO3的物质的量,进而计算Na2CO3的质量.
解答:解:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,
NaHCO3加热分解生成Na2CO3,最后得到的固体为Na2CO3,
配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,
则n(Na+)=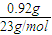 =0.04mol,
=0.04mol,
n(Na2CO3)=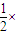 n(Na+)=0.04mol×
n(Na+)=0.04mol× =0.02mol,
=0.02mol,
m(Na2CO3)=0.02mol×106g/mol=2.12g,
故选C.
点评:本题考查混合物的计算,题目难度不大,本题注意加热后固体的成分的判断,根据Na元素守恒计算.
解答:解:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,
NaHCO3加热分解生成Na2CO3,最后得到的固体为Na2CO3,
配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,
则n(Na+)=
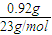 =0.04mol,
=0.04mol,n(Na2CO3)=
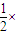 n(Na+)=0.04mol×
n(Na+)=0.04mol× =0.02mol,
=0.02mol,m(Na2CO3)=0.02mol×106g/mol=2.12g,
故选C.
点评:本题考查混合物的计算,题目难度不大,本题注意加热后固体的成分的判断,根据Na元素守恒计算.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
实验室配制100mL 1.0mol/L Na2CO3溶液,下列有关叙述正确的是( )
| A、用托盘天平称取10.6g Na2CO3固体 | B、将Na2CO3固体放入容量瓶中,加水至刻度线 | C、定容时俯视液面,所得溶液浓度偏低 | D、加水时不慎超过刻度线,用胶头滴管直接吸出多余液体 |

 nH2O和NaHCO3的混合物4.0g溶于水,配制成100mL溶液,向其中加入2.0mol/L盐酸至不再产生气体时,消耗盐酸20.0mL,放出气体0.672L(标准状况)。
nH2O和NaHCO3的混合物4.0g溶于水,配制成100mL溶液,向其中加入2.0mol/L盐酸至不再产生气体时,消耗盐酸20.0mL,放出气体0.672L(标准状况)。
