题目内容
4.下列关于晶体的说法中,不正确的是( )①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥晶体根据结构和性质只可分为分子晶体、原子晶体、离子晶体和金属晶体四大类
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6.
| A. | ①②③⑥ | B. | ②③④ | C. | ④⑤⑥ | D. | ②③⑥⑦ |
分析 ①根据晶体和非晶体中微粒的排列特点分析;
②含有金属阳离子的晶体是离子晶体或金属晶体;
③分子晶体的熔、沸点由分子间作用力决定;
④离子晶体中离子半径越小,离子所带电荷越多,晶格能越大;
⑤根据晶胞概念分析;
⑥根据晶体的构成微粒将晶体分类;
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl晶体中配位数为8,NaCl晶体配位数为6.
解答 解:①晶体中粒子在三维空间里呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性,故正确;
②含有金属阳离子的晶体是离子晶体或金属晶体,金属晶体是金属阳离子和自由电子构成的,故错误;
③分子晶体的熔、沸点由分子间作用力决定,与分子中的共价键无关,故错误;
④离子晶体中离子半径越小,离子所带电荷越多,晶格能越大,MgO和NaCl两种晶体中,半径:Mg2+<Na+,且镁离子带电荷多,则MgO的晶格能较大,所以其熔点比较高,故正确;
⑤晶胞是描述晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列,故正确;
⑥根据晶体的构成微粒将晶体分为分子晶体、原子晶体、离子晶体和金属晶体以及混合型晶体,故错误;
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl晶体中阴阳离子的配位数为8,NaCl晶体中阴阳离子的配位数为6,所以CsCl和NaCl晶体中阴、阳离子的配位数不同,故错误.
所以不正确的有②③⑥⑦;
故选D.
点评 本题考查了晶体与非晶体的区别、晶体的构成、晶胞的概念、配位数的判断等,题目涉及的知识点较多,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | 化学反应不一定有分子碰撞 | B. | 发生有效碰撞的分子是活化分子 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 化学反应的活化能一定大于零 |
9.近期埃博拉病毒在非洲各国肆虐,严重威胁了非洲人民的生命.在此期间,环境消毒是极其关键的,常常喷洒一种名为“84”的消毒液,其有效成分为NaClO.下列有关“84”消毒液的说法正确的是( )
| A. | NaClO属于共价化合物 | |
| B. | ClO-与Ca2+、Fe2+、Al3+ 能大量共存 | |
| C. | 1L 0.1mol?L-1NaClO溶液中ClO-的数目为0.1NA | |
| D. | “84”消毒液在空气中久置变质发生了氧化还原反应 |
16.下列物质属于非电解质的是( )
| A. | CO2 | B. | (NH4)2SO4 | C. | Cl2 | D. | CH3COOH |
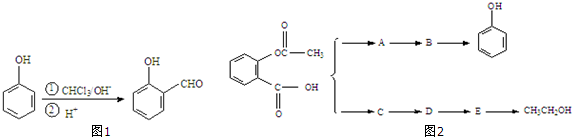
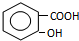 ,B
,B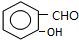 ,C
,C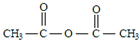 ,DCH3COOH,ECH3CHO.
,DCH3COOH,ECH3CHO.
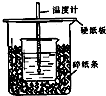 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: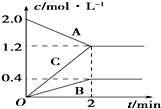 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答: