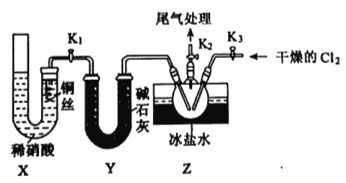
题目内容
【题目】Ⅰ.现有三种短周期元素:①H ②Na ③Cl。
(1)氢原子结构示意图______; ②的单质在③的单质中燃烧,生成物是一种_______化合物(填“离子”或“共价”)。
(2)①与③形成的化合物的电子式是_______________,该化合物中含有___________共价键(填“极性”或“非极性”)。
Ⅱ.现有四种烃分子的球棍模型(如图)。
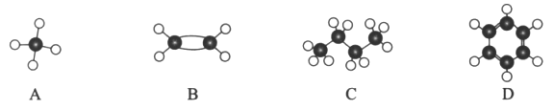
(1)与A互为同系物的是___________(填序号)。
(2)能使酸性高锰酸钾溶液褪色的物质是_____________(填序号)。
(3)C的同分异构体的结构简式是_____________________________。
(4)在光照条件下,A与氯气发生反应生成气态有机物的化学反应方程式是:________。
【答案】 ![]() 离子
离子 ![]() 极性 C B
极性 C B ![]() CH4+Cl2
CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
【解析】Ⅰ.(1).氢元素的核电荷数为1,其原子结构示意图为 ![]() ;钠在氯气中燃烧生成氯化钠,含有离子键。 (2).氢元素和氯元素形成氯化氢,其电子式为
;钠在氯气中燃烧生成氯化钠,含有离子键。 (2).氢元素和氯元素形成氯化氢,其电子式为 ![]() ;该物质含有极性键;Ⅱ.A为甲烷,B为乙烯,C为丁烷,D为苯。(1)和甲烷互为同系物的为丁烷,选C;(2)乙烯能使酸性高锰酸钾溶液褪色;(3).丁烷的同分异构体为2-甲基丙烷,结构简式为
;该物质含有极性键;Ⅱ.A为甲烷,B为乙烯,C为丁烷,D为苯。(1)和甲烷互为同系物的为丁烷,选C;(2)乙烯能使酸性高锰酸钾溶液褪色;(3).丁烷的同分异构体为2-甲基丙烷,结构简式为 ![]() ;(4).甲烷和氯气反应生成一氯甲烷和氯化氢,方程式为: CH4+Cl2
;(4).甲烷和氯气反应生成一氯甲烷和氯化氢,方程式为: CH4+Cl2![]() CH3Cl+HCl。
CH3Cl+HCl。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】电解法生产锰时会产生大量的阳极泥,其主要成分为MnO2和Pb,还含有少量其他金属化合物。下图是回收电解锰阳极泥生产MnCO3的工艺流程。

已知:Al(OH)3、Mn(OH)2、MnCO3的Ksp分别为1.0×10-33、1.9×10-13、2.2×10-11。
(l)“还原酸浸”时氧化产物为CO2,发生反应的化学方程式为____。
(2)“还原酸浸”实验中,锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为 ____ 。

(3)滤液l中的阳离子组成见下表:
组成 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
浓度/(mol·L-1) | 0.85 | 2.4×10-3 | 1.0×10-2 | 2.0×10-3 |
“除杂”时先加MnO2,MnO2的作用为 ___。
再加氨水调节pH使杂质离子沉淀完全,通过计算说明Al3+沉淀完全时Mn2+是否开始沉淀 ___。
(4)“沉锰”时发生反应的离子方程式为 ___。
(5)“沉锰”的关键操作有2点:①将NH4HCO3溶液滴入MnSO4溶液中;②反应终点pH=7。如果颠倒试剂滴加顺序,将MnSO4溶液滴人NH4HCO3,溶液中,或反应终点pH>7可能造成同样的后果,该后果是____;如粜反应终点pH<7,可能的后果是______。
(6)从滤液2中回收得到的副产品的用途为________。