题目内容
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味、遇水反应生成一种氯化物和两种氮化物。某学习小组在实验空用Cl2和NO制备ClNO并测定其纯度,相关实验装置(夹持装置略去)如下图所示。请回答:

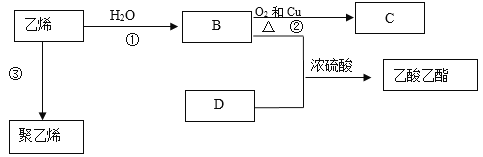
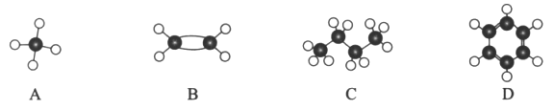
(1)制备C12发生装置可以选用____(填写字母代号),请写出发生反应的离子方程式:____________。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→_______(按气流方向,用小写字母表示)。
(3)实验室可用下图装置制备亚硝酰氯(C1NO):
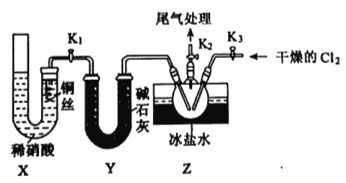
①实验室也可用B装置制备NO,X装置的优点为__________。
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为_______,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为________。
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmolL-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为______(用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(K2CrO4)=1×10-12]
【答案】 A或(B) MnO2+4H++2Cl-![]() Mn2++Cl2+2H2O(或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O f→g→c→b→d→e→j→h 排除装置内空气的干扰,可以随开随用,随关随停 排干净三颈瓶中的空气,防NO和ClNO变质 2ClNO+H2O=2HCl+NO↑+NO2↑
Mn2++Cl2+2H2O(或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O f→g→c→b→d→e→j→h 排除装置内空气的干扰,可以随开随用,随关随停 排干净三颈瓶中的空气,防NO和ClNO变质 2ClNO+H2O=2HCl+NO↑+NO2↑ ![]() ×100%
×100%
【解析】(1)实验室可以选用二氧化锰和浓盐酸加热反应制备氯气,制备C12发生装置可以选用A,也可以选择高锰酸钾或氯酸钾与浓盐酸常温下制备氯气,此时发生装置可以选择B;反应的离子方程式可以是MnO2+4H++2Cl-![]() Mn2++Cl2+2H2O或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O,故答案为:A或(B);MnO2+4H++2Cl-
Mn2++Cl2+2H2O或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O,故答案为:A或(B);MnO2+4H++2Cl-![]() Mn2++Cl2+2H2O或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O;
Mn2++Cl2+2H2O或2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O或ClO3-+6H++5Cl-=3Cl2↑+3H2O;
(2)浓盐酸易挥发,制得的氯气中混有氯化氢和水蒸气,可以选择饱和食盐水除去氯化氢,浓硫酸干燥氯气,收集一瓶干燥的氯气,其连接顺序为:a→f→g→c→b→d→e→j→h,故答案为:f→g→c→b→d→e→j→h;
(3)①实验室制备NO可以选用稀硝酸和铜反应,用B装置和X装置制备NO,X装置的优点有排除装置内空气的干扰,可以随开随用,随关随停,故答案为:排除装置内空气的干扰,可以随开随用,随关随停;
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,目的是排干净三颈瓶中的空气,防NO和ClNO变质,然后进行其他操作,当Z有一定量液体生成时,停止实验,故答案为:排干净三颈瓶中的空气,防NO和ClNO变质;
③X装置中生成的NO中混有水蒸气,碱石灰可以干燥NO,若无装置Y,亚硝酰氯(ClNO)遇水反应生成一种氯化物和两种氮化物,反应的化学方程式为2ClNO+H2O=2HCl+NO↑+NO2↑,故答案为:2ClNO+H2O=2HCl+NO↑+NO2↑;
(4)2ClNO+H2O=2HCl+NO↑+NO2↑,滴定时发生Ag++Cl-= AgCl↓,滴定消耗的AgNO3的物质的量为0.02250L ×cmolL-1=0.02250cmol,则样品中含有氯元素的物质的量=0.02250cmol×![]() =0.2250cmol,因此亚硝酰氯(C1NO)的质量分数=
=0.2250cmol,因此亚硝酰氯(C1NO)的质量分数=![]() ×100%=
×100%=![]() ×100%,故答案为:
×100%,故答案为: ![]() ×100%。
×100%。

【题目】碳酸钙、盐酸是中学化学实验中的常用试剂.
(1)甲同学拟测定CaCO3固体与过量0.1molL﹣1 HCl的反应速率.
①该反应的离子方程式为 .
②设计实验方案:通过测量计算反应速率
(2)乙同学拟用如图装置探究固体表面积和反应物浓度对化学反应速率的影响.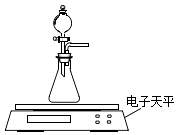
电子天平限选试剂与用品:0.1molL﹣1 HCl、颗粒状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
(i)设计实验方案:在反应物浓度或固体表面积不同的条件下,测定
(要求所测得的数据能直接体现反应速率大小).
(ⅱ) 根据(i)中设计的实验测定方案,拟定实验表格,完整体现实验方案.列出所用试剂的用量、待测物理量;数据用字母a、b、c、d表示.
已知实验1和2探究固体表面积对反应速率的影响;
实验1和3探究反应物浓度对反应速率的影响.
写出表中①﹣⑥所代表的必要数据或物理量
物理量 | V(0.1molL﹣1 HCl)/mL | m(颗粒状CaCO3)/g | m(粉末状CaCO3)/g | V(蒸馏水)/mL | ⑤ | ⑥ |
实验1 | a | b | 0 | c | d | |
实验2 | ① | 0 | ③ | c | d | |
实验3 | c | ② | 0 | ④ | d |