题目内容
【题目】下列说法不正确的是( )
A.在25℃时,将amol?L﹣1的氨水与0.01 mol?L﹣1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl﹣),用含a的代数式表示NH3?H2O的电离常数:Kb= ![]()
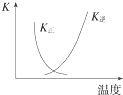
B.在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应生成Z,平衡后测得X、Y的转化率与起始时两物质的物质的量之比n(X)/n(Y>的关系如图所示,则x与Y的反应方程式可表示为:X+3Y?nZ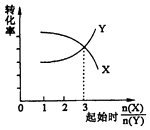
C.某同学在实验室进行了如图所示的实验,则Y中反应的离子方程式为:3CaCO3+2Fe3++3H2O═2Fe(OH)3+3CO2↑+3Ca2+
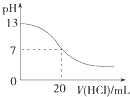
D.将10mL 1 mol?L﹣1Na2CO3溶液逐滴滴加到10mL1mol?L﹣1盐酸中,滴加结束后生成的溶液中有:C(Na+)>c(Cl﹣)>c(CO32﹣)>c(HCO3﹣)
【答案】B
【解析】解:A.在25℃下,平衡时溶液中c(NH4+)=c(Cl﹣)=0.005mol/L,根据物料守恒得c(NH3 . H2O)=(0.5a﹣0.005)mol/L,根据电荷守恒得c(H+)=c(OH﹣)=10﹣7mol/L,溶液呈中性,NH3H2O的电离常数Kb= ![]() =
= ![]() =
= ![]() ,故A正确; B.当反应物的起始物质的量之比等于化学计量数之比,物质的转化率相同,据此由图可知
,故A正确; B.当反应物的起始物质的量之比等于化学计量数之比,物质的转化率相同,据此由图可知 ![]() =3时,转化率相同,即X与Y的化学计量数之比为3:1,故B错误;
=3时,转化率相同,即X与Y的化学计量数之比为3:1,故B错误;
C.氯化铁溶液由于铁离子水解,溶液显酸性,加入碳酸钙,碳酸钙与氢离子反应生成二氧化碳气体,使铁离子的水解平衡正向移动,故反应的离子方程式为:3CaCO3+2Fe3++3H2O═2Fe(OH)3+3CO2↑+3Ca2+ , 故C正确;
D.将10ml 1 molL﹣1Na2CO3溶液逐滴滴加到10ml 1 molL﹣1盐酸中,碳酸钠和盐酸反应生成二氧化碳、水和氯化钠,碳酸钠过量,所得溶液为等物质的量浓度的碳酸钠和氯化钠的混合溶液,碳酸钠电离出钠离子和碳酸根离子,氯化钠电离出钠离子和氯离子,碳酸根离子部分水解生成碳酸氢根离子,故滴加结束后生成的溶液中有:c(Na+)>c(Cl﹣)>c(CO32﹣)>c(HCO3﹣),故D正确;
故选B.
【考点精析】根据题目的已知条件,利用化学平衡状态本质及特征和弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.