题目内容
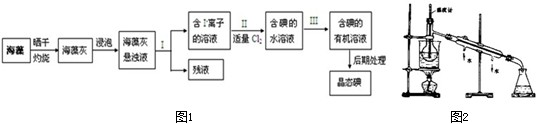
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的过程如图所示: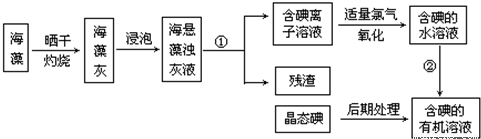
请填写下列空白:
(1)灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是______ (从下列仪器中选出所需的仪器,用标号字母填写在空白处).
A.烧杯 B.瓷坩埚 C.表面皿 D.泥三角 E.酒精灯 F.坩埚钳
(2)指出提取碘的过程中有关的实验操作名称:①______、②______.
(3)提取碘的过程中,不能使用的有机溶剂是______.其原因是______.
A.酒精 B.苯 C.汽油
该提取操作通常在______(仪器名称)中进行,若得到的是含碘的四氯化碳溶液,静置后分层,下层为______色.
(4)设计一个简单的实验,检验提取碘后的水溶液中是否还含有单质碘.请写出该实验的实验步骤、现象及结论______.
(5)“加碘食盐”中的碘主要以碘酸钾形式存在,其中碘元素的化合价是______.
测定“加碘食盐”中碘元素含量的一种方法如下:称取50.0g食盐溶于适量水,加入过量碘化钾和稀硫酸,其反应的化学方程式为:
______KIO3+______KI+______H2SO4→______K2SO4+______I2+______H2O
①配平上述方程式,配平后的系数为:______.还原剂是______.
②实验中,若测得生成3.0×10-5 mol I2,则该食盐中碘元素的含量是______mg/kg.(精确至0.1)
【答案】分析:(1)根据实验操作步骤灼烧来分析用到的实验仪器;
(2)分离固体和液体用过滤;用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来用萃取;萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,据此来选择合适的试剂;
(4)根据碘单质的特性遇淀粉显蓝色来检验;
(5)①根据氧化还原反应中得失电子数相等配平,元素化合价升高的为还原剂;
②依据KIO3+5Kl+3H2SO4═3K2SO4+3I2+3H2O进行计算;
解答:解:(1)灼烧固体物质一般使用(瓷)坩埚,而瓷坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是,瓷坩埚、泥三角、酒精灯、坩埚钳;
故答案为:BDEF;
(2)分离固体和液体用过滤;利用溶质在互不相溶的溶剂里溶解度不同,用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来,这种方法叫做萃取,将碘水中的碘单质萃取出来,选择合适的萃取剂即可,
故答案为:过滤;萃取(分液);
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,酒精与水互溶,所以不能选用;
碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和水都不互溶,且四氯化碳和碘不反应,故可用四氯化碳,若得到的是含碘的四氯化碳溶液,静置后分层,下层为紫(红)色,
故答案为:A;酒精与水互溶;紫(红)色;
(4)淀粉溶液遇碘变蓝色,可用来检验碘单质,所以操作为取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质,
故答案为:取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质;
(5)①该反应中化合价的变化为:KIO3→I2,I元素由+5价→0价,一个KIO3分子得5个电子;KI→I2,I元素由-1价→0价,KI为还原剂,一个KI失一个电子,所以得失电子的最小公倍数为5,KIO3的计量数为1,KI的计量数为5,其它元素根据原子守恒配平,
故答案为:1、5、3、3、3、3;KI;
②KIO3+5Kl+3H2SO4═3K2SO4+3I2+3H2O
1 3
1.0×10-5 3.0×10-5
则50克食盐中含碘元素的物质的量为1.0×10-5mol,1000g食盐中碘元素物质的量为:1.0×10-5mol×20=2.0×10-4mol,1000g食盐中碘元素的质量为:2.0×10-4mol×127g/mol=254×10-4g=25.4mg,所以该食盐中碘元素的含量是25.4mg/kg,
故答案为:25.4;
点评:本题主要考查了实验室里从海藻中提取碘,涉及到的知识点较多,掌握碘元素的有关知识及其计算是解答的关键,题目难度中等.
(2)分离固体和液体用过滤;用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来用萃取;萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,据此来选择合适的试剂;
(4)根据碘单质的特性遇淀粉显蓝色来检验;
(5)①根据氧化还原反应中得失电子数相等配平,元素化合价升高的为还原剂;
②依据KIO3+5Kl+3H2SO4═3K2SO4+3I2+3H2O进行计算;
解答:解:(1)灼烧固体物质一般使用(瓷)坩埚,而瓷坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是,瓷坩埚、泥三角、酒精灯、坩埚钳;
故答案为:BDEF;
(2)分离固体和液体用过滤;利用溶质在互不相溶的溶剂里溶解度不同,用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来,这种方法叫做萃取,将碘水中的碘单质萃取出来,选择合适的萃取剂即可,
故答案为:过滤;萃取(分液);
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,萃取剂与溶质不反应,酒精与水互溶,所以不能选用;
碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和水都不互溶,且四氯化碳和碘不反应,故可用四氯化碳,若得到的是含碘的四氯化碳溶液,静置后分层,下层为紫(红)色,
故答案为:A;酒精与水互溶;紫(红)色;
(4)淀粉溶液遇碘变蓝色,可用来检验碘单质,所以操作为取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质,
故答案为:取少量提取液于试管中,滴加淀粉溶液,若溶液显蓝色,则说明原提取液中有碘单质;
(5)①该反应中化合价的变化为:KIO3→I2,I元素由+5价→0价,一个KIO3分子得5个电子;KI→I2,I元素由-1价→0价,KI为还原剂,一个KI失一个电子,所以得失电子的最小公倍数为5,KIO3的计量数为1,KI的计量数为5,其它元素根据原子守恒配平,
故答案为:1、5、3、3、3、3;KI;
②KIO3+5Kl+3H2SO4═3K2SO4+3I2+3H2O
1 3
1.0×10-5 3.0×10-5
则50克食盐中含碘元素的物质的量为1.0×10-5mol,1000g食盐中碘元素物质的量为:1.0×10-5mol×20=2.0×10-4mol,1000g食盐中碘元素的质量为:2.0×10-4mol×127g/mol=254×10-4g=25.4mg,所以该食盐中碘元素的含量是25.4mg/kg,
故答案为:25.4;
点评:本题主要考查了实验室里从海藻中提取碘,涉及到的知识点较多,掌握碘元素的有关知识及其计算是解答的关键,题目难度中等.

练习册系列答案
相关题目
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海藻中提取碘的流程如下:
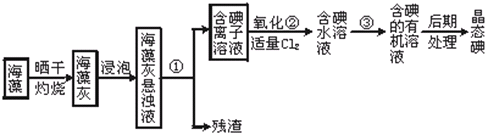
(1)指出提取碘的过程中有关实验操作名称 ① ③
(2)写出过程②中有关反应的离子方程式
(3)提取碘的过程中,可供选择的有机试剂是
A.乙酸 B.苯 C.四氯化碳 D.酒精

(1)指出提取碘的过程中有关实验操作名称 ①
(2)写出过程②中有关反应的离子方程式
(3)提取碘的过程中,可供选择的有机试剂是
A.乙酸 B.苯 C.四氯化碳 D.酒精
| 有机试剂 | 酒精 | 四氯化碳 | 苯 | 乙酸 |
| 毒性 | 无 | 无 | 有 | 无 |
| 水溶性 | 与水以任意比互溶 | 与水互不相溶 | 与水互不相溶 | 与水以任意比互溶 |