题目内容
【题目】某兴趣小组用锡粒制备氯化锡![]() 和氯化亚锡
和氯化亚锡![]() ,流程如下:
,流程如下:
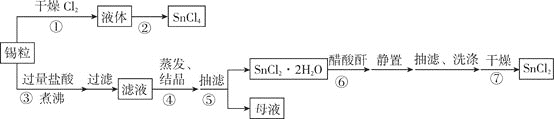
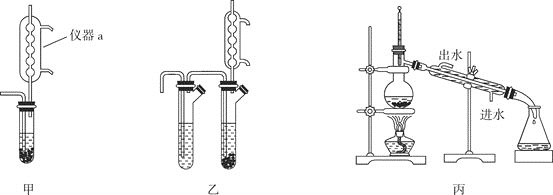
制备![]() 的装置如图:
的装置如图:
已知:![]() 为无色液体,熔点
为无色液体,熔点![]() ,沸点
,沸点![]() ,遇水强烈水解,可溶于乙醇、四氯化碳等。
,遇水强烈水解,可溶于乙醇、四氯化碳等。![]() 为白色晶体,在空气中加热会发生水解及氧化。
为白色晶体,在空气中加热会发生水解及氧化。![]() 为白色晶体,熔点
为白色晶体,熔点![]() ,沸点
,沸点![]() ,易溶于水、乙醇、冰醋酸,极易溶于盐酸。
,易溶于水、乙醇、冰醋酸,极易溶于盐酸。
请回答:
![]() 步骤
步骤![]() 的反应装置如图甲,其中仪器a的作用为________。若用图乙代替图甲作为反应装置,优点是在不拆除装置的情况下,向支管不断填装锡粒大量制备
的反应装置如图甲,其中仪器a的作用为________。若用图乙代替图甲作为反应装置,优点是在不拆除装置的情况下,向支管不断填装锡粒大量制备![]() ,则制备过程中将生成的
,则制备过程中将生成的![]() 转移至蒸馏烧瓶中的简易操作为________。
转移至蒸馏烧瓶中的简易操作为________。
![]() 步骤
步骤![]() 的装置如图丙,此装置存在一处明显的缺陷为________。
的装置如图丙,此装置存在一处明显的缺陷为________。
![]() 步骤
步骤![]() 选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,其理由为________。
选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,其理由为________。
![]() 步骤
步骤![]() 中的反应需在搅拌下进行,该反应的化学方程式为________。
中的反应需在搅拌下进行,该反应的化学方程式为________。
![]() 关于
关于![]() 的制备,下列说法不正确的是________。
的制备,下列说法不正确的是________。
A.步骤![]() 蒸发及步骤
蒸发及步骤![]() 干燥时均需在真空环境下进行
干燥时均需在真空环境下进行
B.步骤![]() 抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,应用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,以提高产率
抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,应用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,以提高产率
C.为提高产品纯度,可在含醋酸酐的冰醋酸中重结晶
D.![]() 在干燥
在干燥![]() 或干燥HCl气流中加热也可得到无水
或干燥HCl气流中加热也可得到无水![]()
E.若步骤![]() 产生的母液较多,可进一步浓缩母液以提高产品纯度
产生的母液较多,可进一步浓缩母液以提高产品纯度
【答案】冷凝回流用橡皮球![]() 洗耳球
洗耳球![]() 从冷凝管上口向装置中鼓气,将液体从左端导管压入蒸馏烧瓶中锥形瓶上口缺少隔绝空气中水蒸气的装置能形成原电池,加快锡与盐酸的反应速率
从冷凝管上口向装置中鼓气,将液体从左端导管压入蒸馏烧瓶中锥形瓶上口缺少隔绝空气中水蒸气的装置能形成原电池,加快锡与盐酸的反应速率![]() BE
BE
【解析】
![]() 步骤
步骤![]() 中的仪器为冷凝管,它的作用是冷凝回流;利用压强原理,将生成的
中的仪器为冷凝管,它的作用是冷凝回流;利用压强原理,将生成的![]() 转移至蒸馏烧瓶中的简易操作为:用橡皮球
转移至蒸馏烧瓶中的简易操作为:用橡皮球![]() 洗耳球
洗耳球![]() 从冷凝管上口向装置中鼓气,将液体从左端导管压入蒸馏烧瓶中;
从冷凝管上口向装置中鼓气,将液体从左端导管压入蒸馏烧瓶中;
![]() 步骤
步骤![]() 的装置是用来制取氯化亚锡
的装置是用来制取氯化亚锡![]() 的,由于氯化亚锡
的,由于氯化亚锡![]() 易溶于水,所有制取后锥形瓶不能敞口,否则水蒸气就会进入锥形瓶,故此装置存在一处明显的缺陷为:锥形瓶上口缺少隔绝空气中水蒸气的装置;
易溶于水,所有制取后锥形瓶不能敞口,否则水蒸气就会进入锥形瓶,故此装置存在一处明显的缺陷为:锥形瓶上口缺少隔绝空气中水蒸气的装置;
![]() 锡比铂金属性活泼,在盐酸中可形成原电池,加快反应速率,所以步骤
锡比铂金属性活泼,在盐酸中可形成原电池,加快反应速率,所以步骤![]() 选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,故答案为:能形成原电池,加快锡与盐酸的反应速率;
选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,故答案为:能形成原电池,加快锡与盐酸的反应速率;
![]() 骤
骤![]() 中的反应是氯化亚锡晶体与醋酸酐反应,生成醋酸和氯化亚锡,该反应的化学方程式为:
中的反应是氯化亚锡晶体与醋酸酐反应,生成醋酸和氯化亚锡,该反应的化学方程式为:![]() ;
;
![]() 因为
因为![]() 为白色晶体,在空气中加热会发生水解及氧化,所以步骤
为白色晶体,在空气中加热会发生水解及氧化,所以步骤![]() 蒸发及步骤
蒸发及步骤![]() 干燥时均需在真空环境下进行,选项A正确;B. 抽滤是用于分离粒径较细的沉淀与溶剂,利用抽气泵使抽滤瓶中的压强降低,加快过滤速度,步骤
干燥时均需在真空环境下进行,选项A正确;B. 抽滤是用于分离粒径较细的沉淀与溶剂,利用抽气泵使抽滤瓶中的压强降低,加快过滤速度,步骤![]() 抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,不能提高产率,选项B错误;C.因为
抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,不能提高产率,选项B错误;C.因为![]() 为白色晶体,易溶于水、乙醇、冰醋酸,所以为提高产品纯度,可在含醋酸酐的冰醋酸中重结晶,选项 C正确;D.因为
为白色晶体,易溶于水、乙醇、冰醋酸,所以为提高产品纯度,可在含醋酸酐的冰醋酸中重结晶,选项 C正确;D.因为![]() 在空气中加热会发生水解及氧化,所以在干燥
在空气中加热会发生水解及氧化,所以在干燥![]() 中加热可隔绝空气,在干燥HCl气流中加热可抑制氯化亚锡发生水解,也可得到无水
中加热可隔绝空气,在干燥HCl气流中加热可抑制氯化亚锡发生水解,也可得到无水![]() ,选项D正确;E.若步骤
,选项D正确;E.若步骤![]() 产生的母液中主要成分为盐酸,进一步浓缩母液对产品纯度没有影响,选项 E错误。故答案为:BE。
产生的母液中主要成分为盐酸,进一步浓缩母液对产品纯度没有影响,选项 E错误。故答案为:BE。

 名校课堂系列答案
名校课堂系列答案【题目】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白
族周期 | IA | IIA | IIIA | IV A | V A | VI A | VII A | O |
一 | A | |||||||
二 | B | C | ||||||
三 | D | E | F | G | H | I | ||
四 | K | J | ||||||
(1)这11种元素中化学性质最不活泼的是___,金属性最强的是____.(写元素符号)
(2)第三周期元素中,原子半径最大的元素是(稀有气体元素除外)____,离子半径最小的是____,单质氧化性最强的元素是____.(写元素符号)
(3)J的简单离子的结构示意图__.
(4)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)_____________________.
(5)比较G、H两元素的最高价氧化物对应水化物的酸性____>_____.比较C、G两元素的气态氢化物稳定性____>_____.(写化学式)
(6)C和D的单质在点燃条件下生成化合物的电子式为__,它属于____(离子或共价)化合物.
(7)用电子式表示A和G所形成的简单化合物的形成过程__.
【题目】化石能源的脱硫处理是环保热点问题。
用臭氧处理燃煤烟气脱硫的主要反应如下:![]()
![]() ,向1L反应装置充入
,向1L反应装置充入![]() 和
和![]() ,经过相同反应时间t后剩余
,经过相同反应时间t后剩余![]() 的物质的量与温度关系如图所示:
的物质的量与温度关系如图所示:
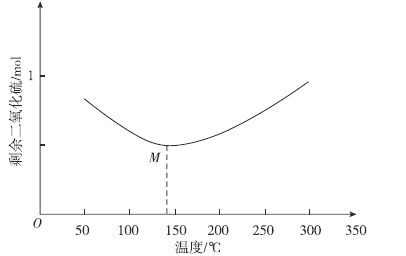
已知臭氧会转化成氧气:![]() ,在上述反应条件下臭氧分解率与温度关系如下:
,在上述反应条件下臭氧分解率与温度关系如下:
温度 | 50 | 100 | 150 | 200 | 250 | 300 |
| 0 | 0 | 0 | 4 | 20 | 81 |
![]() 关于脱硫的主要反应,下列说法错误的是______________。
关于脱硫的主要反应,下列说法错误的是______________。
![]() 时,缩小反应装置的体积可以提高相同时间t内
时,缩小反应装置的体积可以提高相同时间t内![]() 的转化率
的转化率
![]() 点该反应处于平衡状态
点该反应处于平衡状态
![]() 随温度的升高,正反应速率变大,逆反应速率减小
随温度的升高,正反应速率变大,逆反应速率减小
![]() 以后随着温度升高,
以后随着温度升高,![]() 的物质的量增多的原因可能是______________________。
的物质的量增多的原因可能是______________________。
![]() 已知
已知![]() 时
时![]() 的平衡常数
的平衡常数![]() ,求该温度下反应
,求该温度下反应![]() 的平衡常数
的平衡常数![]() __________。
__________。
![]() 其他条件不变,经过相同反应时间
其他条件不变,经过相同反应时间![]() ,在图中画出剩余
,在图中画出剩余![]() 的物质的量在
的物质的量在![]() 点温度范围内的关系趋势图____________。
点温度范围内的关系趋势图____________。
![]() 烟气脱硫后续还需用碱液吸收
烟气脱硫后续还需用碱液吸收![]() 形成
形成![]() ,溶液pH为
,溶液pH为![]() 之间时
之间时![]() 在电解池阴极上被还原成连二硫酸根
在电解池阴极上被还原成连二硫酸根![]() ,写出该电极反应式:___________________________。
,写出该电极反应式:___________________________。
【题目】非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
⑴ O2-的电子式为___________;
⑵ O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________(写化学式,任写两种);
⑶ CH3OH在常温下为液态,沸点高于乙烷的主要原因是__________________________;
⑷ Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
危险性 |
|
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用____________________________。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是_________________。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中
c(Cl-) : c(ClO-)=11 : 1时,则c(ClO-) :c(ClO3-)比值等于_____________。
⑸ 镁是一种较活泼的金属, Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6g。请写出该水解反应方程式___________________________。