题目内容
常温下,下列各组离子或分子在指定溶液中一定能大量共存的是( )
| A、0.1mol?L-1 NaOH溶液中:K+、Na+、SO42-、CO32- |
| B、加入KSCN溶液显红色的溶液中:K+、NH4+、Cl-、H2S |
| C、使甲基橙呈红色的溶液中:NH4+、Na+、SiO32-、Cl- |
| D、能溶解Al(OH)3的溶液中:Ca2+、Cl-、K+、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.碱性溶液中该组离子之间不反应;
B.加入KSCN溶液显红色的溶液,含铁离子;
C.使甲基橙呈红色的溶液,显酸性;
D.能溶解Al(OH)3的溶液为酸或强碱溶液.
B.加入KSCN溶液显红色的溶液,含铁离子;
C.使甲基橙呈红色的溶液,显酸性;
D.能溶解Al(OH)3的溶液为酸或强碱溶液.
解答:
解:A.碱性溶液中该组离子之间不反应,可大量共存,故A正确;
B.加入KSCN溶液显红色的溶液,含铁离子,与H2S发生氧化还原反应,不能共存,故B错误;
C.使甲基橙呈红色的溶液,显酸性,H+、SiO32-结合生成沉淀,不能共存,故C错误;
D.能溶解Al(OH)3的溶液为酸或强碱溶液,酸或碱溶液中不能大量存在HCO3-,不能共存,故D错误;
故选A.
B.加入KSCN溶液显红色的溶液,含铁离子,与H2S发生氧化还原反应,不能共存,故B错误;
C.使甲基橙呈红色的溶液,显酸性,H+、SiO32-结合生成沉淀,不能共存,故C错误;
D.能溶解Al(OH)3的溶液为酸或强碱溶液,酸或碱溶液中不能大量存在HCO3-,不能共存,故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A、升高温度,溶液的pH增大 |
| B、室温时,此酸的电离平衡常数约为1×10-7 |
| C、该溶液的pH=4 |
| D、升高温度,电离平衡常数增大 |
下列叙述正确的是( )
| A、浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 |
| B、XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强 |
| C、非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
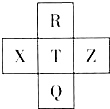 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A、非金属性:Z<T<X |
| B、R与Q的电子数相差26 |
| C、气态氢化物稳定性:R<T<Q |
| D、最高价氧化物的水化物的酸性:T>Q |
下列说法正确的是( )
| A、SiH4比CH4稳定 |
| B、P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的强 |
| C、Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D、O2-半径比F-的小 |
在下列条件下,一定能大量共存的离子组是( )
| A、强酸性溶液中:Al3+、K+、Mg2+、Cl-、SO42- |
| B、pH=13的溶液中:Cl-、HCO3-、NO3-、NH4+ |
| C、c(Fe3+)=0.1mol?L-1的溶液中:Na+、SCN-、Cl-、Br- |
| D、强碱性溶液中:ClO-、SO42-、SO32-、Na+ |
下列离子方程式书写正确的是( )
| A、氯化铝溶液和过量的氨水反应:Al3++4NH3?H2O═AlO2-+4NH4+ |
| B、少量的CO2通入NaOH溶液中:CO2+2OH-═CO32-+H2O |
| C、醋酸加入小苏打溶液中:HCO3-+H+═CO2↑+H2O |
| D、硫化钠的水解:S2-+2H2O?H2S+2OH- |