��Ŀ����
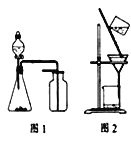
����Ŀ��ij�о���ѧϰС���������ͼ��ʾʵ��װ��(�г�����ʡ��)��ȡ����İ�������֤NH3���л�ԭ�ԣ���ش��������⣺

��1��ʵ�����Ʊ������ж��ַ�����������NH4C1��Ca(OH)2��Ӧ��ȡNH3������е����巢��װ��___________(�Ӣ���ѡ��)����Ũ��ˮ����ʯ�ҷ�ӦҲ����ȡNH3����Ӧ�Ļ�ѧ����ʽΪ__________
��2��װ�ñ������ռ�NH3��Ӧ������__________(����a������b�����ӳ�������ƿ�ײ���װ������ʢ�ŵ��Լ�Ϊ__________��װ�ü�������Ϊ____________(�����㣩��
��3����װ�ö��к�ɫ�����죬��װ����������Ϊ_________
��4���о�С���ͬѧͨ�����ۡ���������Ϊ��ַ�Ӧ�����ɵĺ�ɫ���������Cu��Cu2O����ߵĻ���ͨ����������֪��Cu2O+2H+=Cu+Cu2++H2O��Ϊ̽������ijɷ֣�������������ַ�����
I. ��ͬѧȡ������ɫ������ϡ�����ϣ����յõ���ɫ��Һ���ɴ��Ʋ��ɫ��������Cu2O��
����Լ�ͬѧʵ����Ƶ�������__________���������Ҫ�����ֽ���)��
��Cu2O��ϡ���ᷴӦ�����ӷ���ʽΪ_____________
��.��ͬѧ��Ϊ����Ҫ�����κλ�ѧ�Լ���ֻ��Ҫ�������ɵĺ�ɫ�������������Ϊxg������ȷ������ɷ֣���xȡֵ��ΧΪ _____ʱ�����������м���Cu������Cu2O��
���𰸡�B CaO+NH3��H2O =Ca(OH)2 + NH3 �� b ��ʯ�� ����û�з�Ӧ���NH3����ֹ������ˮ��������װ������ ��ɫ�����Ϊ��ɫ ����������ΪCu��Cu2O���ܱ�ϡ��������ΪCu2+ 3Cu2O+14H++2NO��=6Cu2++2NO ��+7H2O 12.8<x<14.4
��������
����NH4C1��Ca(OH)2�ڼ��������·�Ӧ��ȡNH3����˵õ����е����巢��װ�ã���Ũ��ˮ����ʯ�ҷ�Ӧ����NH3���������ơ�
�ư������ܶȱȿ���С��װ�ñ������ռ�NH3������Ӧ�����Ϸ���װ������Ҫ�Ǹ��ﰱ�����������ʢ�ŵ��Լ�Ϊ��ʯ�ң�װ�ü�������Ϊ����û�з�Ӧ���NH3����ֹ������ˮ��������װ�����С�
����װ�ö��к�ɫ�����죬��������ˮ��ˮ�������뵽װ����������Ϊ��ɫ�����Ϊ��ɫ��
��I.��������ͭ����������ͭ����ϡ���ᷴӦ����ͭ���ӣ���˼�ͬѧʵ����Ƶ������Dz�������
��Cu2O��ϡ���ᷴӦ�����ӷ���ʽΪ3Cu2O+14H++2NO��=6Cu2++2NO ��+7H2O��
����16g����ͭ�����ʵ���Ϊ0.2mol��ȫ����Ϊͭ���ʼ�����Ϊ0.2mol��64g/mol = 12.8g��������ͭȫ����Ϊ������ͭʱ�������ʵ���Ϊ0.1mol������Ϊ0.1mol��144g/mol = 14.4g����˵�xȡֵ��ΧΪ12.8<x<14.4ʱ�����������м���Cu������Cu2O��
����NH4C1��Ca(OH)2�ڼ��������·�Ӧ��ȡNH3����˼��е����巢��װ��B����Ũ��ˮ����ʯ�ҷ�Ӧ����NH3���������ƣ���Ӧ�Ļ�ѧ����ʽΪCaO+NH3��H2O =Ca(OH)2 + NH3 �����ʴ�Ϊ��B��CaO+NH3��H2O =Ca(OH)2 + NH3 ����
�ư������ܶȱȿ���С��װ�ñ������ռ�NH3��Ӧ������b�ӳ�������ƿ�ײ���װ������Ҫ�Ǹ��ﰱ�����������ʢ�ŵ��Լ�Ϊ��ʯ�ң�װ�ü�������Ϊ����û�з�Ӧ���NH3����ֹ������ˮ��������װ�����У��ʴ�Ϊ��b����ʯ�ң�����û�з�Ӧ���NH3����ֹ������ˮ��������װ�����С�
����װ�ö��к�ɫ�����죬��������ˮ��ˮ�������뵽װ����������Ϊ��ɫ�����Ϊ��ɫ���ʴ�Ϊ����ɫ�����Ϊ��ɫ��
��I.��������ͭ����������ͭ����ϡ���ᷴӦ����ͭ���ӣ���Լ�ͬѧʵ����Ƶ������Dz���������ΪCu��Cu2O���ܱ�ϡ��������ΪCu2+���ʴ�Ϊ������������ΪCu��Cu2O���ܱ�ϡ��������ΪCu2+��
��Cu2O��ϡ���ᷴӦ�����ӷ���ʽΪ3Cu2O+14H++2NO��=6Cu2++2NO ��+7H2O���ʴ�Ϊ��3Cu2O+14H++2NO��=6Cu2++2NO ��+7H2O��
����16g����ͭ�����ʵ���Ϊ0.2mol��ȫ����Ϊͭ���ʼ�����Ϊ0.2mol��64g/mol = 12.8g��������ͭȫ����Ϊ������ͭʱ�������ʵ���Ϊ0.1mol������Ϊ0.1mol��144g/mol = 14.4g����˵�xȡֵ��ΧΪ12.8<x<14.4ʱ�����������м���Cu������Cu2O���ʴ�Ϊ��12.8<x<14.4��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�