��Ŀ����
��ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ����
������������⣺
��1����D�ǵ��ʣ�����A����ͬһ���壬��
�ٷ�Ӧ�Ļ�ѧ����ʽ��______��
��D��ԭ�ӽṹʾ��ͼ��______��
��D���ʵ�һ����Ҫ��;��______��
��2����BΪ��ɫ���壬DΪ���廯�����
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��______��
�������ù�ҵƷ�Ĺ���Ӧ������______�Ͻ��ĵط���
��ʵ���Ҽ���C�ķ�����______��
��3����B��һ���д̼�����ζ�����壬��
��B�ķ�����״��______��
��ʵ���ҽ��д�ʵ��ʱ���������д������̲�������˵�������������̵�ԭ��______��
�ۻ�����C��һ������������У���һ�������·�����Ӧ����������������ѹǿ��С��ԭ����
����д���÷�Ӧ�Ļ�ѧ����ʽ______��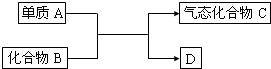
������������⣺
��1����D�ǵ��ʣ�����A����ͬһ���壬��
�ٷ�Ӧ�Ļ�ѧ����ʽ��______��
��D��ԭ�ӽṹʾ��ͼ��______��
��D���ʵ�һ����Ҫ��;��______��
��2����BΪ��ɫ���壬DΪ���廯�����
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��______��
�������ù�ҵƷ�Ĺ���Ӧ������______�Ͻ��ĵط���
��ʵ���Ҽ���C�ķ�����______��
��3����B��һ���д̼�����ζ�����壬��
��B�ķ�����״��______��
��ʵ���ҽ��д�ʵ��ʱ���������д������̲�������˵�������������̵�ԭ��______��
�ۻ�����C��һ������������У���һ�������·�����Ӧ����������������ѹǿ��С��ԭ����
| 2 |
| 3 |

��1��D��Aͬ���壬A���û���D���Ҹ÷�Ӧ����Ҫ��Ӧ�������Ԫ�����ڱ�����֪A��C��D��Si����2C+SiO2
2CO+Si��Si��ԭ�ӽṹʾ��ͼ��
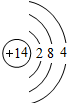
���赥�ʵ�һ����Ҫ��;���ư뵼����ϣ��ʴ�Ϊ��2C+SiO2
2CO+Si��

���ư뵼����ϣ�
��2���ٻ�����BΪ��ɫ���壬��ѧ�εĻ�ɫ���廯������AgI��������ȣ������ڹ�ҵ������ֻ�����û���������Ũ���ᣬ��A��������B��FeS2��C��SO2����˻�ѧ����ʽΪ4FeS2+11O2
2Fe2O3+SO2���ʴ�Ϊ��4FeS2+11O2
2Fe2O3+SO2����
�ڸ÷�Ӧ���ڹ�ҵ�������ᣬ����Ũ�����Ǹ�ʴƷ������ɱ��ϸߣ���Σ���Դ���˽���ʱӦ��ѡ����ʹ��Ũ�����ܼ��ĵط�������ҵ�����е��������ģ��ʴ�Ϊ���������ģ�
����Ϊ�����Ͷ���������ʹƷ����Һ��ɫ���������ö���ѧ���ʵIJ��ʵ���Ҽ����������ͨ�����ã�������Cͨ��Ʒ����Һ�У���Һ��ɫ������Һ���ȣ��ָֻ���ɫ��
�ʴ�Ϊ��������Cͨ��Ʒ����Һ�У���Һ��ɫ������Һ���ȣ��ָֻ���ɫ��
��3���ٸ÷�ӦΪ��ҵ������ת����ϵ����ʵ��������ʵ���а��̣������ѧ�ΰ�����ӷ�����������������̵�֪ʶ����֪�÷�Ӧ�ǹ�ҵ�ϰ�����������ȡ����ķ�Ӧ����
4NH3+5O2
4NO+6H2O�����B��NH3��C��NO�����������������Σ��ʴ�Ϊ�������Σ�
��ʵ���ҽ��д˷�Ӧ��NO�ᱻ������������ΪNO2��������ˮ��Ӧ�������ᣬ�����백����Ӧ��������臨������������̣��������ɵ�NO���屻������������NO2��NO2��ˮ��Ӧ���ɵ�������NH3��Ӧ�������������̣��ʴ�Ϊ�����ɵ�NO���屻������������NO2��NO2��ˮ��Ӧ���ɵ�������NH3��Ӧ�������������̣�
��NO���ܱ�������һ�������¿��Էֽ�Ϊ����������һ���������������ķ�ӦΪ3NO=NO2+N2O�����ڴ���2NO2?N2O4�������������ѹǿ��С��ԭ����
��
�ʴ�Ϊ��3NO=NO2+N2O��
| ||

���赥�ʵ�һ����Ҫ��;���ư뵼����ϣ��ʴ�Ϊ��2C+SiO2
| ||

���ư뵼����ϣ�
��2���ٻ�����BΪ��ɫ���壬��ѧ�εĻ�ɫ���廯������AgI��������ȣ������ڹ�ҵ������ֻ�����û���������Ũ���ᣬ��A��������B��FeS2��C��SO2����˻�ѧ����ʽΪ4FeS2+11O2
| ||
| ||
�ڸ÷�Ӧ���ڹ�ҵ�������ᣬ����Ũ�����Ǹ�ʴƷ������ɱ��ϸߣ���Σ���Դ���˽���ʱӦ��ѡ����ʹ��Ũ�����ܼ��ĵط�������ҵ�����е��������ģ��ʴ�Ϊ���������ģ�
����Ϊ�����Ͷ���������ʹƷ����Һ��ɫ���������ö���ѧ���ʵIJ��ʵ���Ҽ����������ͨ�����ã�������Cͨ��Ʒ����Һ�У���Һ��ɫ������Һ���ȣ��ָֻ���ɫ��
�ʴ�Ϊ��������Cͨ��Ʒ����Һ�У���Һ��ɫ������Һ���ȣ��ָֻ���ɫ��
��3���ٸ÷�ӦΪ��ҵ������ת����ϵ����ʵ��������ʵ���а��̣������ѧ�ΰ�����ӷ�����������������̵�֪ʶ����֪�÷�Ӧ�ǹ�ҵ�ϰ�����������ȡ����ķ�Ӧ����
4NH3+5O2
| ||
| �� |
��ʵ���ҽ��д˷�Ӧ��NO�ᱻ������������ΪNO2��������ˮ��Ӧ�������ᣬ�����백����Ӧ��������臨������������̣��������ɵ�NO���屻������������NO2��NO2��ˮ��Ӧ���ɵ�������NH3��Ӧ�������������̣��ʴ�Ϊ�����ɵ�NO���屻������������NO2��NO2��ˮ��Ӧ���ɵ�������NH3��Ӧ�������������̣�
��NO���ܱ�������һ�������¿��Էֽ�Ϊ����������һ���������������ķ�ӦΪ3NO=NO2+N2O�����ڴ���2NO2?N2O4�������������ѹǿ��С��ԭ����
| 2 |
| 3 |
�ʴ�Ϊ��3NO=NO2+N2O��

��ϰ��ϵ�д�
�����Ŀ
 ��ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ����
��ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ����

 2NH3��g������H��0���仯ѧƽ�ⳣ��K��t�Ĺ�ϵ���±�������֪K=
2NH3��g������H��0���仯ѧƽ�ⳣ��K��t�Ĺ�ϵ���±�������֪K=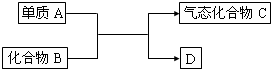 ��ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ����
��ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ���� ����д���÷�Ӧ�Ļ�ѧ����ʽ______��
����д���÷�Ӧ�Ļ�ѧ����ʽ______�� ����д���÷�Ӧ�Ļ�ѧ����ʽ ��
����д���÷�Ӧ�Ļ�ѧ����ʽ ��