题目内容
7.在20℃时,在100g水中溶解11.1g K2SO4恰好达到饱和,此时饱和溶液的密度为1.08g/cm3,求此饱和溶液的质量分数与物质的量浓度.分析 饱和溶液中w%=$\frac{{m}_{质}}{{m}_{液}}$,结合c=$\frac{1000ρw}{M}$计算.
解答 解:20℃时,在100g水中溶解11.1g K2SO4恰好达到饱和,则此饱和溶液的质量分数为$\frac{11.1g}{100g+11.1g}$×100%≈9.99%,
c=$\frac{1000ρw}{M}$=$\frac{1000×1.08×\frac{11.1g}{111.1g}×100%}{174}$=0.62mol/L,
答:此饱和溶液的质量分数为9.99%,物质的量浓度为0.62mol/L.
点评 本题考查物质的量浓度的计算,为高频考点,把握浓度、质量分数的计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
18.下列现象与氢键有关的是( )
①NH3的熔、沸点比ⅤA族其他元素的氢化物高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④氟化氢比碘化氢稳定
⑤液态氟化氢的化学式有时可以写成(HF)n的形式.
①NH3的熔、沸点比ⅤA族其他元素的氢化物高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④氟化氢比碘化氢稳定
⑤液态氟化氢的化学式有时可以写成(HF)n的形式.
| A. | ①②④⑤ | B. | ①②③④ | C. | ①②③⑤ | D. | 全部 |
12.下列实验操作错误的是( )
| A. | 欲除去溴水中混有的少量碘,加入苯进行萃取 | |
| B. | 除去碳酸钠中的少量碳酸氢钠,加热固体 | |
| C. | 除去CO2中的少量SO2:通过盛有足量NaHCO3溶液的洗气瓶 | |
| D. | 提取溶解在水中的少量碘:加入CCl4,振荡、静置、分层后取出有机层再分离 |
6.关于H2→H2O,CO→CO2,Mg→MgO三种物质的转化过程中,下列说法不正确的是( )
| A. | 都能通过化合反应实现 | B. | 都能通过置换反应实现 | ||
| C. | 都能通过与单质反应实现 | D. | 变化前后元素化合价都发生了改变 |
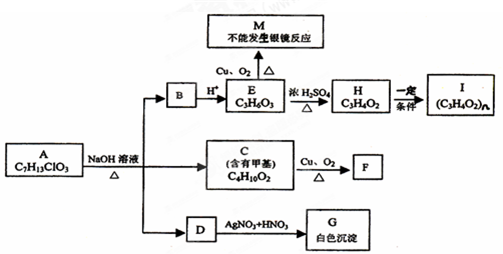
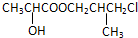 、
、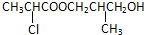
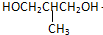 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$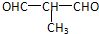 +2H2O;
+2H2O;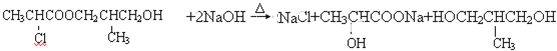 ;
;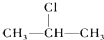 +NaOH$→_{醇}^{△}$CH3-CH═CH2+NaCl+H2O烯烃A在一定条件下可以按图进行反应
+NaOH$→_{醇}^{△}$CH3-CH═CH2+NaCl+H2O烯烃A在一定条件下可以按图进行反应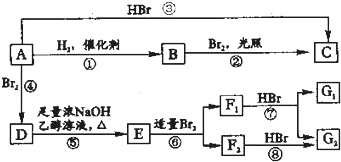
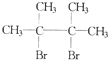 .A的结构简式为(CH3)2C=C(CH3)2.
.A的结构简式为(CH3)2C=C(CH3)2.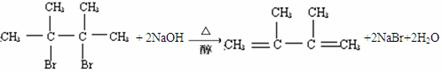 .
.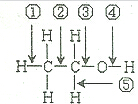 乙醇的分子结构为(如图):乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.
乙醇的分子结构为(如图):乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.