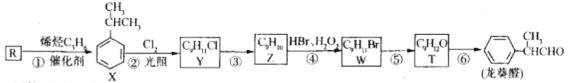
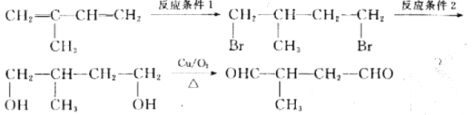
题目内容
【题目】在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)![]()
![]() mol/(L·min)
mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<![]() mol/(L·min)
mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
【答案】C
【解析】
试题0~6min时间内,△c(H2O2)=0.002mol÷0.01L=0.2mol/L,所以v(H2O2)=0.2mol/L÷6min![]()
![]() mol/(L·min), A正确;随着反应的进行,H2O2的浓度逐渐减小,反应速率减慢,B正确;6min时,c(H2O2)=0.002mol÷0.01L=0.2mol/L, C错误;6min时,H2O2分解率为:
mol/(L·min), A正确;随着反应的进行,H2O2的浓度逐渐减小,反应速率减慢,B正确;6min时,c(H2O2)=0.002mol÷0.01L=0.2mol/L, C错误;6min时,H2O2分解率为:![]() =50%, D正确。
=50%, D正确。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+ Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 该温度下此反应的平衡常数K = 1.44
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 反应前2 min的平均速率v(Z) = 2.0×10-3 mol/(L·min)
D. 其他条件不变,再充入0.2 mol X,平衡时Y的体积分数增大
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |