题目内容
某课外学习小组的同学设计了如图的装置,以验证SO2的氧化性、还原性和漂白性。回答以下问题
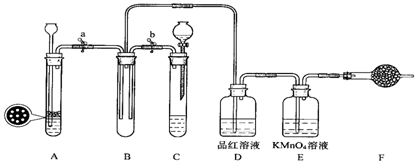
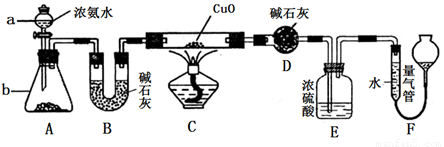
(1)用Na2SO3固体和硫酸溶液制取SO2气体,应选用________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是_____________。小组同学发现产生气体的速率缓慢,可能的原因是_________________。
(2)课外学习小组的同学用FeS固体和稀硫酸制取H2S气体,反应的方程式为___________________________。
(3)SO2气体通过D装置时现象是_______,通过E装置时现象是_____________;SO2与H2S在B装置中反应,现象是____________________________。
(4)F中盛有碱石灰,其作用是___________________________________。
(2)课外学习小组的同学用FeS固体和稀硫酸制取H2S气体,反应的方程式为___________________________。
(3)SO2气体通过D装置时现象是_______,通过E装置时现象是_____________;SO2与H2S在B装置中反应,现象是____________________________。
(4)F中盛有碱石灰,其作用是___________________________________。
(1)C;Na2SO3是可溶性固体,不能用具“随开随用”功能的装置;Na2SO3已部分变质、硫酸溶液太稀
(2)FeS + H2SO4 = FeSO4 + H2S↑
(3)溶液红色褪去;溶液紫色褪去;管壁变模糊,有淡黄色固体生成
(4)吸收尾气(H2S或SO2),避免污染空气
(2)FeS + H2SO4 = FeSO4 + H2S↑
(3)溶液红色褪去;溶液紫色褪去;管壁变模糊,有淡黄色固体生成
(4)吸收尾气(H2S或SO2),避免污染空气

练习册系列答案
相关题目