题目内容
为了验证碱金属元素和第三周期金属元素金属性的相对强弱,某课外活动小组的同学设计如下实验,请根据要求回答下列问题:
(1)取少量金属钠和金属钾分别放入盛 的烧杯中,观察到钾的现象是 ;由此得出的结论是 。
(2)将镁条打磨至银白色后放入盛有上述物质的试管中, 明显现象(填“有”或“没有”), 后(填操作名称)可观察到有大量气泡产生,反应的化学方程式是 ;
(3)将打磨好的镁条和铝条分别放入盛 的试管中,观察到明显的现象,铝条反应的离子方程式是 ,由(1)(2)(3)可得出的结论是 ;
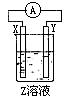
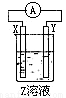
(4)某同学在学习了电化学基础知识后,设计了如图所示(X、Y分别是Mg、Al)的装置进行实验,发生氧化反应的负极金属性强,但发现镁条上有气体产生,由此得出了与实验(3)相反的结论,你知道这位同学所用的Z溶液是
,其负极的电极反应式是
(1)水(1分),在水面上迅速游动并着火(1分),同主族元素从上到下金属性增强(1分);
(2)没有(1分),加热至沸腾(1分),Mg+2H2O=Mg(OH)2+H2↑(2分);
(3)稀盐酸(或稀硫酸其他合理答案也给分)(1分),2Al+6H+=2Al3++3H2↑(2分),同周期从左到右金属性减弱(1分);
(4)NaOH溶液(或氢氧化钠)(2分),Al+4OH--3e-=AlO2-+2H2O
【解析】略

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案