题目内容
将2.5g金属混合物的粉末跟足量的盐酸反应,生成2.24 L H2(标况),则此金属混合物可能是( )
| A.Mg和Al | B.Al和Fe | C.Fe和Zn | D.Zn和Cu |
B
试题分析:用极端假设法解。若2.5g金属全是Mg、Al、Fe、Zn、Cu,与足量盐酸生成氢气物质的量分别为0.104mol、0.139mol、0.045mol、0.038mol、0mol。所以符合题意的组合为Al和Fe。
点评:此类问题宜采用极端假设法解题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
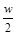 g水,可得到2a%的NaCl溶液(
g水,可得到2a%的NaCl溶液(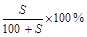 >2a%)
>2a%)