题目内容
【题目】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
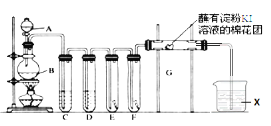
(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式__________________________。
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是________________________,对比E和F中现象的差异可得出的结论及解释是________________________________。
(3)试管C和D中试剂各为_____________________________。
(4)装置G处发生反应的离子方程式为_______________________________。
(5)用离子方程式表示试剂X的作用_________________________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式__________________。
②需“密闭保存”的原因____________________________________________。
【答案】MnO2+4H++2Cl-![]() Mn2++Cl2↑+ 2H2O E中干布条不褪色,F中湿布条褪色 Cl2没有漂白性,HClO有漂白性 饱和食盐水、浓硫酸 Cl2+2I-=2Cl-+I2 Cl2+2OH-=Cl-+ClO-+ H2O Cl-+ ClO-+ 2H+= Cl2↑+ H2O NaClO溶液与空气中CO2反应生成HClO,HClO不稳定易分解。
Mn2++Cl2↑+ 2H2O E中干布条不褪色,F中湿布条褪色 Cl2没有漂白性,HClO有漂白性 饱和食盐水、浓硫酸 Cl2+2I-=2Cl-+I2 Cl2+2OH-=Cl-+ClO-+ H2O Cl-+ ClO-+ 2H+= Cl2↑+ H2O NaClO溶液与空气中CO2反应生成HClO,HClO不稳定易分解。
【解析】
实验室用浓盐酸与二氧化锰加热反应制备氯气,浓盐酸具有挥发性,制备的氯气中含有氯化氢、水,依次通过盛有饱和食盐水、浓硫酸的洗气瓶除去杂质,依次通过干燥有色布条、湿润有色布条验证氯气是否具有漂白性,再通过G装置验证氯气的氧化性,氯气有毒,能够与氢氧化钠溶液反应,可以用氢氧化钠溶液吸收尾气。据此分析解答。
(1)MnO2与浓盐酸在加热条件下发生氧化还原反应生成氯气、氯化锰和水,反应的方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+ 2H2O;
Mn2++Cl2↑+ 2H2O;
(2)由于氯气本身没有漂白性,氯气与水反应产生了具有漂白性的HClO,而具有漂白性,所以看到的现象是:E中干燥的布条不褪色,F中湿润的布条褪色;
(3)在实验室中用浓盐酸与二氧化锰加热反应制备氯气,浓盐酸具有挥发性,使制备的氯气中混有杂质氯化氢、水蒸气,先通过盛有饱和食盐水的C装置除去HCl杂质,再通过盛有浓硫酸的D装置洗气瓶干燥氯气,除去水蒸气,就可防止水蒸气对氯气漂白性检验造成干扰,以便于检验氯气的性质;
(4)氯气具有强的氧化性,在溶液中与碘化钾反应生成单质碘,碘遇到淀粉变蓝,反应的离子方程式为Cl2+2I-=2Cl-+I2;
(5)氯气有毒不能直接排放到空气中,由于氯气能够与碱反应,产生容易溶于水的物质,所以可以用氢氧化钠溶液作吸收试剂,吸收过量的氯气,反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O;
(6) ①家庭中常用消毒液与洁厕灵混合,其中次氯酸根离子与氯离子在酸性条件下会发生氧化还原反应产生有毒的氯气,离子方程式:Cl-+ClO-+2H+=Cl2↑+H2O;
②由于酸性H2CO3>HClO,消毒液有效成分次氯酸钠与空气中的二氧化碳和水生成的次氯酸,次氯酸不稳定,见光容易分解,所以应该密封保存。

【题目】(题文)由下列实验及现象不能推出相应结论的是
实验 | 现象 | 结论 | |
A | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3固体受热分解,产生的NH3与水反应生成的氨水显碱性 |
B | 向2支盛有1 mL相同浓度AgNO3溶液的试管中分别加入3滴相同浓度的KCl和KI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 |
|
C | 向苯酚钠溶液中通入CO2 | 溶液变浑浊 | 相同条件下,碳酸的酸性一定比苯酚强 |
D | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液中一定存在Na+和K+ |
A. A B. B C. C D. D