题目内容
12.下列化学用语正确的是( )| A. | C02分子比例模型示意图: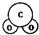 | B. | O原子核外电子轨道表示式: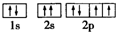 | ||
| C. | Ca2+电子排布式:ls22s23s23p6 | D. | K原子结构示意图: |
分析 A、C02分子为直线形结构;
B、2s轨道的电子的自旋方向应该相反;
C、Ca原子质子数为20,则Ca2+核外有18个电子;
D、K原子质子数为19.
解答 解:A、C02分子为直线形结构,故A错误;
B、O为8号元素,2s轨道的两个电子的自旋方向应该相反,故B错误;
C、Ca原子质子数为20,则Ca2+核外有18个电子,电子排布式为ls22s23s23p6,故C正确;
D、K原子质子数为19,最外层电子数要小于8,故D错误;
故选C.
点评 本题考查了常见化学用语的书写判断,题目难度中等,注意掌握原子结构示意图、比例模型、电子排布式、轨道表示式等化学用语的概念及表示方法,选项A为易错点.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
2.现有部分短周期元素的性质或原子结构如下表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置第三周期ⅥA族;
②B元素原子结构示意图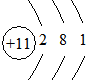 ;
;
③C单质分子的电子式 ;用电子式表示A和B元素组成的化合物的形成过程
;用电子式表示A和B元素组成的化合物的形成过程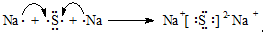 ;
;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素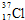 .
.
(2)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bde(填选项序号).
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是NaOH(写化学式).
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:BaSO4;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl(或Ba2++SO2+H2O2=BaSO4↓+2H+);
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:1:2.
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置第三周期ⅥA族;
②B元素原子结构示意图
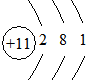 ;
;③C单质分子的电子式
 ;用电子式表示A和B元素组成的化合物的形成过程
;用电子式表示A和B元素组成的化合物的形成过程 ;
;④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
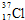 .
.(2)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bde(填选项序号).
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是NaOH(写化学式).
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:BaSO4;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl(或Ba2++SO2+H2O2=BaSO4↓+2H+);
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:1:2.
20.下列离子方程式书写不正确的是( )
| A. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| B. | 氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| C. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | NO2溶于水:3NO2+H2O═2H++2NO3-+NO |
7.能实现 转变为的
转变为的 操作是( )
操作是( )
 转变为的
转变为的 操作是( )
操作是( )| A. | 先与NaOH溶液共热,再通人足量C02 | B. | 先与NaOH溶液共热,冉通人足量HC1 | ||
| C. | 先与稀H2S04共热,加人足量Na2CO3 | D. | 先与稀H2S04共热,加人足量NaOH |
17.华裔科学家高琨因“在光纤传输信息领域中的突破性成就”获得2009年诺贝尔物理学奖,下列关于硅材料的说法正确的是( )
| A. | 光纤的主要成分是高纯度的单质硅 | |
| B. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| C. | 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | 28Si、29Si、30Si互为同位素 |
18.下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为2:1的有( )
| A. | 对苯二甲酸 | B. | 丙酸 | C. | 乙二醇 | D. | 乙酸 |
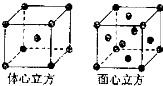 Mn、Fe均为第四周期过渡元素.请回答下列问题:
Mn、Fe均为第四周期过渡元素.请回答下列问题: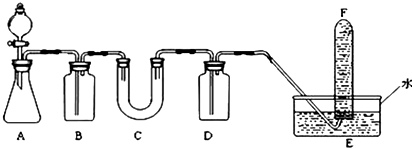
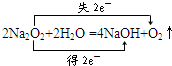 ,所以
,所以