题目内容
爱迪生蓄电池在充电和放电时发生的反应:Fe+ NiO2+2H2O Fe(OH)2+Ni(OH)2,
Fe(OH)2+Ni(OH)2,
下列该蓄电池推断错误的是:
①放电时,Fe参与负极反应,NiO2参与正极反应
②充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-=" Fe" + 2OH-
③放电时,电解质溶液中的阴离子向正极方向移动
④放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤蓄电池的电极必须浸入某种碱性电解质溶液中
 Fe(OH)2+Ni(OH)2,
Fe(OH)2+Ni(OH)2,下列该蓄电池推断错误的是:
①放电时,Fe参与负极反应,NiO2参与正极反应
②充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-=" Fe" + 2OH-
③放电时,电解质溶液中的阴离子向正极方向移动
④放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤蓄电池的电极必须浸入某种碱性电解质溶液中
| A.只有③ | B.③④ | C.④⑤ | D.①②⑤ |
B
放电相当于原电池,充电相当于电解池。在原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应。在电解池中阳极失去电子发生氧化反应,阴极得到电子,发生还原反应。根据所给反应式可知向右是原电池,向左是电解池。在原电池中阳离子向正极移动,阴离子向负极移动,③不正确。因为放电时的生成物是氢氧化物,所以溶液不可能显酸性即④不正确,应为Fe + 2OH――2e-= Fe(OH)2,所以答案是B。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
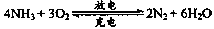

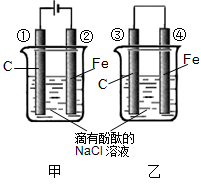
 2CO2+4H2O。(已知甲醇的标准燃烧热为-725.76kJ ·mol-1)
2CO2+4H2O。(已知甲醇的标准燃烧热为-725.76kJ ·mol-1)
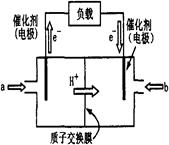
 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数表达式K= ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常K将 (填增大、减小、不变),其反应的正反应速率将 (填增大、减小、不变);逆反应速率将 (填增大、减小、不变);温度升高 (填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数表达式K= ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常K将 (填增大、减小、不变),其反应的正反应速率将 (填增大、减小、不变);逆反应速率将 (填增大、减小、不变);温度升高 (填有利或不利于)电池将化学能转化为电能。 +b kJ·mol-1。若常温下一定量的甲醇完全燃烧生成液态水释放出了1451.52 kJ的能量,则等质量的甲醇利用图示装置理论上可提供 mol电子的电量。
+b kJ·mol-1。若常温下一定量的甲醇完全燃烧生成液态水释放出了1451.52 kJ的能量,则等质量的甲醇利用图示装置理论上可提供 mol电子的电量。