题目内容
据报道,N5是破坏力极强的炸药之一,18O2是比黄金还贵的物质.下列说法正确的是( )
| A、N5和N2互为同位素 |
| B、18O2的摩尔质量为36 |
| C、原子半径:N<18O |
| D、2N5═5N2是化学变化 |
考点:核素,同素异形体
专题:原子组成与结构专题
分析:A.同位素是指:质子数相同中子数不同的同种元素的不同核素;
B.摩尔质量的单位是g/mol;
C.同周期从左到右原子半径逐渐减小;
D.判断物理变化与化学变化的依据:是否有新物质生成.
B.摩尔质量的单位是g/mol;
C.同周期从左到右原子半径逐渐减小;
D.判断物理变化与化学变化的依据:是否有新物质生成.
解答:
解:A.N5和N2 是由同种元素组成的性质不同的单质,互为同素异形体,故A错误;
B.18O2的摩尔质量为36g/mol,故B错误;
C.同周期从左到右原子半径逐渐减小,N原子半径比18O原子半径大,故C错误;
D.N5和N2不是同种物质,所以2N5=5N2是化学变化,故D正确;
故选:D.
B.18O2的摩尔质量为36g/mol,故B错误;
C.同周期从左到右原子半径逐渐减小,N原子半径比18O原子半径大,故C错误;
D.N5和N2不是同种物质,所以2N5=5N2是化学变化,故D正确;
故选:D.
点评:本题考查同位素、同素异形体的判断,注意二者研究对象不同,同位素研究的是原子,同素异形体研究的是单质,题目难度不大.

练习册系列答案
相关题目
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
⑤碱性(同浓度)Ca(OH)2>Ba(OH)2 ⑥与同浓度稀硫酸反应的速率:Mg>Al
⑦氧化性Br2>F2 ⑧熔点:Si3N4>NaCl>SiI4 ⑨沸点:NH3>PH3>AsH3.
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力:OH->CH3COO->Cl-
⑤碱性(同浓度)Ca(OH)2>Ba(OH)2 ⑥与同浓度稀硫酸反应的速率:Mg>Al
⑦氧化性Br2>F2 ⑧熔点:Si3N4>NaCl>SiI4 ⑨沸点:NH3>PH3>AsH3.
| A、①③⑦⑨ | B、②④⑥⑧ |
| C、①④⑥⑨ | D、②③⑤⑦ |
(双选)下列物质在浓H2SO4作用下能发生消去反应的是( )
| A、CH3OH |
| B、(CH3)3COH |
| C、(CH3)3CCH2OH |
D、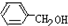 |
E、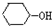 |
为说明氯比硫的非金属性强,下列事实可作依据的是( )
| A、HCl的溶解性强于H2S |
| B、氯的最高价为+7价 |
| C、H2S中的S2-能被Cl2氧化 |
| D、HClO的氧化性强于H2SO4 |
1.28g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到448mL气体(标况).将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是( )
| A、168mL |
| B、224mL |
| C、336mL |
| D、504mL |
按微粒的半径从小到大顺序排列的是( )
| A、Cl、S、P |
| B、N、O、F |
| C、Al、Mg、Na |
| D、K、Na、Li |
下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
| A、使用冰箱保存食物,是利用了化学反应速率理论 |
| B、化学平衡理论是研究怎样使用有限原料多出产品 |
| C、使用催化剂,可加快反应速率,目的是提高生产效率 |
| D、化学反应速率理论是研究怎样提高原料转化率 |
氰气的化学式为(CN)2,结构式为N≡C-C≡N,性质与卤素相似,下列叙述正确的是( )
| A、该分子不能发生加成反应 |
| B、分子中N≡C键的键长大于C-C键的键长 |
| C、分子中含有3个σ键和4个π键 |
| D、不和氢氧化钠溶液发生反应 |
由黄铁矿炼铜的过程中发生了反应:Cu2S+2Cu2O
6Cu+SO2↑,下列叙述正确的是( )
| ||
| A、该反应从氧化还原反应的电子转移看,与SO2+2H2S═3S+2H2O是同一反应类型 | ||||
| B、该反应中,氧元素氧化了硫元素 | ||||
C、该反应从氧化还原反应的电子转移角度看,与6NO2+8NH3
| ||||
| D、该反应中,Cu2S既是还原剂又是氧化剂 |