题目内容
8.设NA为阿伏伽德罗常数,下列叙述正确的是( )| A. | 1L pH=1的乙酸溶液中H+数小于0.1NA | |
| B. | 标准状况下,22.4L乙醇的分子数为NA | |
| C. | 28g乙烯和丙烯所含碳氢键的数目为4NA | |
| D. | 1 mol 甲基所含的电子数为10NA |
分析 A.pH=1的溶液中乙酸氢离子浓度为0.1mol/L,1L该溶液中含有0.1mol氢离子;
B.标准状况下,乙醇的状态不是气体;
C.乙烯和丙烯的最简式为CH2,根据最简式进行计算含有H原子的物质的量,从而得出形成碳氢键的物质的量;
D.甲基为中性原子团,甲基中含有9个电子.
解答 解:A.1L pH=1的乙酸溶液中含有氢离子的物质的量为:0.1mol/L×1L=0.1mol,该溶液中H+数为0.1NA,故A错误;
B.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C.28g乙烯和丙烯的混合气体中含有28个最简式CH2,含有最简式的物质的量为:$\frac{28g}{14g/mol}$=2mol,2mol最简式中含有4molH原子,则含有碳氢键的物质的量为4mol,每个氢原子形成1个碳氢键,则混合物中所含碳氢键的数目为4NA,故C正确;
D.1mol甲基中含有9mol电子,所含的电子数为9NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,B为易错点,注意标况下乙醇不是气体.

练习册系列答案
相关题目
16. 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | 第二份溶液中最终溶质为FeSO4 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 原混合酸中NO3- 物质的量为0.1 mol | |
| D. | H2SO4 浓度为2.5 mol•L-1 |
19.下列描述正确的是( )
| A. | “冰,水为之,而寒于水”说明相同质量的水和冰,冰的能量高 | |
| B. | 水加热到很高的温度都难以分解,主要原因是水分子间可以形成氢键的缘故 | |
| C. | 增大反应物浓度,可增大单位体积内活化分子数,使单位时间内有效碰撞次数增加 | |
| D. | 同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
16.某课外小组设计的实验室制取乙酸乙酯的装置如图所示.已知:
 ①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关物质的沸点如下表所示:
请回答:
(1)若用同位素18O表示反应产物是分子中的氧原子,请写出反应的化学方程式(标明18O在反应物中的位置):CH3COOH+CH3CH218OH$?_{△}^{浓硫酸}$CH3CO18OC2H5+H2O.
(2)分液漏斗A中应加入的试剂为浓硫酸,圆底烧瓶B中应加入少量碎瓷片,目的为防止暴沸.
(3)球形干燥管C的作用为防止倒吸、冷凝.若反应前向D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(4)从D中分离出乙酸乙酯的操作名称为分液;这样得到乙酸乙酯中常含有一定量的乙醇、乙醚和水,欲得到较纯净的乙酸乙酯,应先加入无水氯化钙,目的是分离出乙醇和水;最后进行蒸馏,收集77℃左右的馏分,得到比较纯净的乙酸乙醇.
 ①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH②有关物质的沸点如下表所示:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)若用同位素18O表示反应产物是分子中的氧原子,请写出反应的化学方程式(标明18O在反应物中的位置):CH3COOH+CH3CH218OH$?_{△}^{浓硫酸}$CH3CO18OC2H5+H2O.
(2)分液漏斗A中应加入的试剂为浓硫酸,圆底烧瓶B中应加入少量碎瓷片,目的为防止暴沸.
(3)球形干燥管C的作用为防止倒吸、冷凝.若反应前向D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是溶液分层,上层无色油体液体,下层溶液颜色变浅.
(4)从D中分离出乙酸乙酯的操作名称为分液;这样得到乙酸乙酯中常含有一定量的乙醇、乙醚和水,欲得到较纯净的乙酸乙酯,应先加入无水氯化钙,目的是分离出乙醇和水;最后进行蒸馏,收集77℃左右的馏分,得到比较纯净的乙酸乙醇.
3.新装住房里的装饰材料(如胶合板)会释放出一种刺激性气味的气体,它是居室空气污染的主要来源.该气体是( )
| A. | CH3Cl | B. | NH3 | C. | HCHO | D. | SO2 |
13.下列有关化学用语正确的是( )
| A. | N2的电子式:N??N | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| C. | S2-的结构示意图: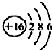 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3=Fe3++SO${\;}_{4}^{2-}$ |
17.下列各组金属的冶炼最适合用H2或CO把它从化合物中还原出来的是( )
| A. | Ca、Mg | B. | Al、Fe | C. | Hg、Ag | D. | Fe、Cu |
 如图所示,若电解5min时铜电极增重2.16g,试回答:
如图所示,若电解5min时铜电极增重2.16g,试回答: