题目内容
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
| | A | B | C | D |
| 实验 | 用CCl4提取碘水中的I2 | 分离乙醇中的I2 | 加热分解 MgCl2?6H2O得到 纯净的MgCl2 | 配制100mL 0.1000mol/L K2Cr2O7溶液 |
| 装置或仪器 | 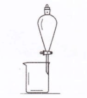 | 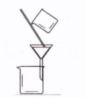 | 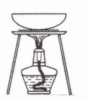 | 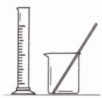 |
A
试题分析:CCl4不溶于水,密度比水大,I2微溶于水,易溶于CCl4,因此可用CCl4提取碘水中的I2,故A正确;I2易溶于乙醇,过滤不能分离乙醇中的碘单质,根据二者互溶但沸点相差较大的性质,应用蒸馏分离提纯,故B错误;加热不仅能使MgCl2?6H2O分解为MgCl2和H2O,而且能使MgCl2彻底水解为受热易分解的Mg(OH)2固体和易挥发的HCl气体,Mg(OH)2受热分解为高熔沸点的MgO固体和易挥发的H2O,因此不能得到纯净的MgCl2,故C错误;配制100mL0.1000mol/LK2Cr2O7溶液需要的仪器有烧杯、玻璃棒、量筒、100mL量筒、胶头滴管,不能缺少100mL量筒和胶头滴管,故D错误。

练习册系列答案
相关题目
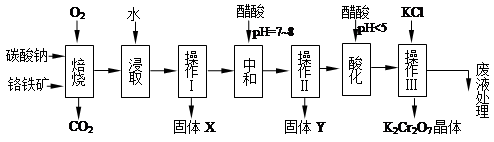
 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑; 2CrO42-+2H+
2CrO42-+2H+ Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。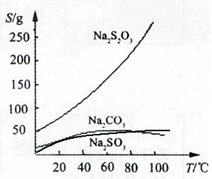
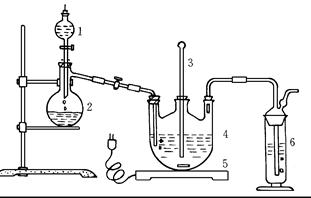
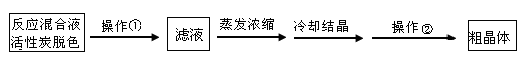

 ×100%”进行计算。由此分析步骤5中滴定反应的离子方程式为 。
×100%”进行计算。由此分析步骤5中滴定反应的离子方程式为 。