��Ŀ����
����Ŀ����ͼ��ʾ�����仯������һ�������µ�ת����ϵ��
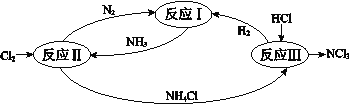
��1�����ݷ�ӦI����500����20MPaʱ����N2��H2ͨ�뵽���Ϊ2 L���ܱ������У���Ӧ�����и������ʵ����ʵ����仯����ͼ��ʾ:

��1��10 min����NH3��ʾ�÷�Ӧ��ƽ�����ʣ�v(NH3)= ��
��2����10~20min��NH3Ũ�ȱ仯��ԭ������� (����ĸ)��
a.���˴���
b.�����¶�
c.����NH3�����ʵ���
��3���ÿ��淴Ӧ�ﵽƽ��ı�־��_______(����ĸ)��
a��3v(H2)�� = 2v(NH3)��
b�����������ܶȲ�����ʱ��仯
c�������ڵ���ѹǿ������ʱ����仯
d�� N2��H2��NH3�ķ�����֮��Ϊ1��3��2
��4����һ��ƽ��ʱ��ƽ�ⳣ��K1�� (����ѧ����ʽ��ʾ)��
��5����ӦI��N2(g)+3H2(g)![]() 2NH3(g) ��H=�C92.4 kJmol��1
2NH3(g) ��H=�C92.4 kJmol��1
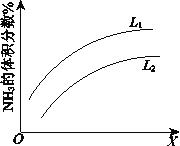
��ͼ��ʾ��ӦI��ƽ��������NH3������������¶Ȼ�ѹǿ�仯�����ߣ�ͼ��L(L1��L2)��X�ֱ�����¶Ȼ�ѹǿ������X��������____________(��¶ȡ���ѹǿ��)���ж�L1��L2�Ĵ�С��ϵ��˵������_______ ��
��6����ӦII����һ����ӦΪ
2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ��H=�C462 kJmol��1
��֪��![]()
�Ͽ�1 mol H�CN����Ͽ�1 mol H�CCl�������������ԼΪ_________ kJ��
���𰸡���1��v(NH3)=0.005mol/(L��min)
��2��a��3��c��4��![]()
��5��ѹǿ��L1��L2,�ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ��ѹǿ��ͬʱ���¶����ߣ�ƽ�������ƶ����������������С��6��41
��������
�����������1����Ӧ����=![]() =0.005mol/(L��min)��
=0.005mol/(L��min)��
��2����ͼ��֪��0-10��������n(N2)=0.025mol��2=0.05mol��10-20��������n��(N2)=0.025mol��4=0.1mol������֮�ȵ������ʵ���֮�ȣ����ԣ�0-10������10��20��������ʱ����У�N2�ķ�Ӧ����֮��Ϊ0.05mol��0.1mol=1��2����ͼ���֪��������ʵ����仯���죬��10minʱ�仯�������ģ�20min��ƽ��ʱ����n��(N2)=0.025mol��4=0.1mol����n(H2)=0.025mol��12=0.3mol����n(NH3)=0.025mol��8=0.2mol�����ʵ����仯֮�ȵ��ڻ�ѧ������֮�ȣ������������ʵ��������ӱ�����ͬ��˵��10min���ܸı��������ʹ�ô������ʴ�Ϊa��
��3����ӦN2(g)+3H2(g)=2NH3��a����2v(H2)�� = 3v(NH3)��ʱ������Ϊƽ����жϣ��ʴ���b�����������������䣬�����������������ܶ�ʼ�ղ��������ܶȲ�����ʱ��仯������˵��ƽ�⣬��������c��������ǰ����������ʵ����б仯��˵��ѹǿʱ��������ѹǿ������ʱ����仯��˵��ƽ�⣬����ȷ��d��N2��H2��NH3�ķ�����֮��Ϊ1��3��2�κ�ʱ�̶��������ʴ���
��4����ѧƽ�ⳣ������������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�������ƽ�ⳣ��K=![]() =
=![]() ��
��
��5��N2(g)+3H2(g)2NH3(g)��H=-92kJmol-1Ϊ���ȷ�Ӧ���������¶�ƽ�������ƶ���ǰ�ڵ����������С����ͼ��ì�ܣ�������ѹǿ��ƽ���������ƶ�������������������ʸı�����Ϊѹǿ��ѹǿ��ͬʱ���¶����ߣ�ƽ�������ƶ����������������С��L1��L2��
��6����1molH-N����Ϊx��1molH-Cl����Ϊy��������H=��Ӧ�����֮��-���������֮�ͣ�-462=6x+3��243-(945+6y)��x-y=41kJ��

 ����������������ϵ�д�
����������������ϵ�д�
