题目内容
在通常条件下,下列各组物质的性质排列正确的是( )
分析:A.从元素的非金属性强弱判断;.
B.从气体常温常压下在水中的溶解度来判断;
C.从烷烃同系物的熔沸点规律来分析;
D.从同周期元素非金属性的递变规律来思考.
B.从气体常温常压下在水中的溶解度来判断;
C.从烷烃同系物的熔沸点规律来分析;
D.从同周期元素非金属性的递变规律来思考.
解答:解:A.同周期从左到右非金属性越来越强,氢化物越来越稳定,即热稳定性:HF>H2O>NH3,故A正确;
B.根据气体在水中的溶解度,常温常压下,1体积水能分别溶解500体积HCl、40体积SO2、700体积NH3,即水溶性:HCl>NH3>SO2,故B不正确;
C.对烷烃同系物来说,其碳原子数越大,其沸点越高,即乙烷<戊烷<丁烷,故C不正确;
D.同周期从左到右最高价氧化物对应水化物的酸性越来越强,即>H3PO4<H2SO4<HClO4,故D不正确;
故选A.
B.根据气体在水中的溶解度,常温常压下,1体积水能分别溶解500体积HCl、40体积SO2、700体积NH3,即水溶性:HCl>NH3>SO2,故B不正确;
C.对烷烃同系物来说,其碳原子数越大,其沸点越高,即乙烷<戊烷<丁烷,故C不正确;
D.同周期从左到右最高价氧化物对应水化物的酸性越来越强,即>H3PO4<H2SO4<HClO4,故D不正确;
故选A.
点评:本题从多方面考查了元素非金属性的递变规律,气体的溶解性,烷烃的物理性质等,具有一定的综合性,能从多个角度考查学生对基础知识的掌握情况.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
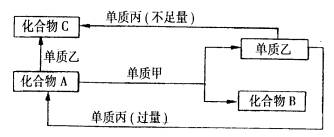
 A、B、C是中学化学中常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质;这些化合物和单质间存在如图所示转化关系(这些转化关系都不需要使用催化剂),回答下列问题:
A、B、C是中学化学中常见的无机物,且各由两种元素组成;甲、乙、丙是三种常见的单质;这些化合物和单质间存在如图所示转化关系(这些转化关系都不需要使用催化剂),回答下列问题:
 (2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).
(2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).