题目内容
在四种化合物①NaHCO3、②Al(OH)3、③(NH4)2S、④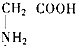 中,跟盐酸和氢氧化钠溶液都能反应的是( )
中,跟盐酸和氢氧化钠溶液都能反应的是( )A.只有②④
B.只有①②
C.只有①②③
D.①②③④
【答案】分析:根据物质间的反应进行判断,中学常见的既能与酸反应又能与碱反应的物质主要有:
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应.以此解答本题.
解答:解:①、NaHCO3溶液能与酸反应生成二氧化碳气体,与碱反应生成碳酸钠,故①正确;
②、Al(OH)3 属于两性氢氧化物,既能与酸反应,生成Al3+离子,又能与碱反应生成AlO2-离子,②正确;
③、(NH4)2S属于弱酸弱碱盐,既能与酸反应,生成H2S气体,又能与碱反应,生成NH3,故③正确;
④、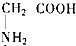 是氨基酸,有酸性基-COOH,能与碱反应;有碱性基-NH2,能与酸反应,故④正确;
是氨基酸,有酸性基-COOH,能与碱反应;有碱性基-NH2,能与酸反应,故④正确;
故选D.
点评:本题考查物质的性质,明确物质的组成来判断物质之间的反应是解答本题的关键,注意在平时的学习中对基础知识的积累和规律归纳.
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应.以此解答本题.
解答:解:①、NaHCO3溶液能与酸反应生成二氧化碳气体,与碱反应生成碳酸钠,故①正确;
②、Al(OH)3 属于两性氢氧化物,既能与酸反应,生成Al3+离子,又能与碱反应生成AlO2-离子,②正确;
③、(NH4)2S属于弱酸弱碱盐,既能与酸反应,生成H2S气体,又能与碱反应,生成NH3,故③正确;
④、
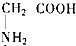 是氨基酸,有酸性基-COOH,能与碱反应;有碱性基-NH2,能与酸反应,故④正确;
是氨基酸,有酸性基-COOH,能与碱反应;有碱性基-NH2,能与酸反应,故④正确;故选D.
点评:本题考查物质的性质,明确物质的组成来判断物质之间的反应是解答本题的关键,注意在平时的学习中对基础知识的积累和规律归纳.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
(14分)下表为一元素周期表(空白,未填元素)根据要求填空。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ② | ③ | ④ |
|
|
| ⑤ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 丙 |
|
| 丁 |
| 甲 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 乙 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑴ 在上面元素周期表中,全部是金属元素的区域为 (填字母代号)
A.甲 B.乙 C.丙 D.丁
⑵用实线画出金属与非金属的分界线(在答题卷图上完成)。
⑶已知R元素的某种原子的质量数为31,且原子核内质子数比中子数少1,请在答题卷中的周期表中标出“R” 元素的位置(在答题卷图上完成)。
⑷在我们常用的周期表中,①元素的位置比较尴尬,它是第1列的唯一非金属元素。有人认为也可把①元素放在VIIA族,支持这个观点的物质是___ _______。
A.HF B.H+ C.NaH D.H2O2
⑸由①②③④四种元素形成的原子个数比为5:1:1:3一种离子化合物的化学式为__ ____;该化合物与过量⑤的氧化物的水化物微热时反应的离子方程式是 ;
若用球棍模型表示①和④形成的化合物的分子结构,应该是 。

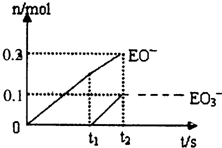 (2011?丹东模拟)有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
(2011?丹东模拟)有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表: