题目内容
X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的化学方程式是______.
(3)Y与R相比,非金属性较强的是______(用元素符号表示),下列事实能证明这一结论的是______(选填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是______.
(5)甲、乙是上述部分元素的最高价氧化物的水化物,且甲+乙→丙+水.若丙的水溶液呈碱性,则丙的化学式是______.
【答案】分析:X、Y、Z、M、R、Q是短周期主族元素,X阳离子核外无电子,则X为H元素;Y的化合价主要为-4,+4,是无机非金属材料的主角,则Y为Si元素;Z焰色反应呈黄色,则Z为Na元素;R的主要化合价为-1,+7,则R为Cl元素;Q主要化合价为+3价,原子半径Na>Q>Cl,则Q为Al元素;M的主要化合价为-2价,为第ⅥA族元素,原子半径M<Cl,则M为O元素,然后利用元素的单质及其化合物的性质来解答.
解答:解:X、Y、Z、M、R、Q是短周期主族元素,X阳离子核外无电子,则X为H元素;Y的化合价主要为-4,+4,是无机非金属材料的主角,则Y为Si元素;Z焰色反应呈黄色,则Z为Na元素;R的主要化合价为-1,+7,则R为Cl元素;Q主要化合价为+3价,原子半径Na>Q>Cl,则Q为Al元素;M的主要化合价为-2价,为第ⅥA族元素,原子半径M<Cl,则M为O元素,
即X为H元素;Y为Si元素;Z为Na元素;R为Cl元素;Q为Al元素;M为O元素.
(1)R为Cl元素,核外有17个电子,核外电子排布为2、8、7,所以Cl元素处于第三周期ⅦA族;
R在自然界中有质量数为35和37的两种核素,中子数不同,二者互为同位素,故答案为:第三周期ⅦA族;同位素;
(2)Z为Na元素,钠与水反应生成氢氧化钠和氢气,反应方程式为2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(3)Y为Si元素,R为Cl元素.同周期自左而右,非金属性减弱,所以非金属性Si<Cl;
a.常温下Y的单质呈固态,R的单质呈气态,状态不能说明元素的非金属性强弱,故a错误;
b.非金属越强,氢化物越稳定,稳定性XR>YX4,说明X的非金属性强,故b正确;
c.Y与R形成的化合物中Y呈正价,说明X吸引电子能力强,X的非金属性强,故c正确.
故答案为:Cl;bc;
(4)Y为Si元素,同周期自左而右,原子半径减小,所以原子半径Al>Si>Cl,即大于0.099nm小于0.143nm,
故答案为:大于0.099nm小于0.143nm;
(5)Y为Si元素;Z为Na元素;R为Cl元素;Q为Al元素;其高价氧化物的水化物,分别为硅酸、氢氧化钠、高氯酸、氢氧化铝.甲+乙→丙+水,丙为盐,丙的水溶液呈碱性,则丙为强碱弱酸盐,则丙为NaAlO2 或Na2SiO3,故答案为:NaAlO2 或Na2SiO3.
点评:本题考查结构、性质与元素、物质的推断、元素周期律等,难度中等,关键清楚元素周期律的变化规律、物质的性质,注意基础知识的掌握与运用.
解答:解:X、Y、Z、M、R、Q是短周期主族元素,X阳离子核外无电子,则X为H元素;Y的化合价主要为-4,+4,是无机非金属材料的主角,则Y为Si元素;Z焰色反应呈黄色,则Z为Na元素;R的主要化合价为-1,+7,则R为Cl元素;Q主要化合价为+3价,原子半径Na>Q>Cl,则Q为Al元素;M的主要化合价为-2价,为第ⅥA族元素,原子半径M<Cl,则M为O元素,
即X为H元素;Y为Si元素;Z为Na元素;R为Cl元素;Q为Al元素;M为O元素.
(1)R为Cl元素,核外有17个电子,核外电子排布为2、8、7,所以Cl元素处于第三周期ⅦA族;
R在自然界中有质量数为35和37的两种核素,中子数不同,二者互为同位素,故答案为:第三周期ⅦA族;同位素;
(2)Z为Na元素,钠与水反应生成氢氧化钠和氢气,反应方程式为2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(3)Y为Si元素,R为Cl元素.同周期自左而右,非金属性减弱,所以非金属性Si<Cl;
a.常温下Y的单质呈固态,R的单质呈气态,状态不能说明元素的非金属性强弱,故a错误;
b.非金属越强,氢化物越稳定,稳定性XR>YX4,说明X的非金属性强,故b正确;
c.Y与R形成的化合物中Y呈正价,说明X吸引电子能力强,X的非金属性强,故c正确.
故答案为:Cl;bc;
(4)Y为Si元素,同周期自左而右,原子半径减小,所以原子半径Al>Si>Cl,即大于0.099nm小于0.143nm,
故答案为:大于0.099nm小于0.143nm;
(5)Y为Si元素;Z为Na元素;R为Cl元素;Q为Al元素;其高价氧化物的水化物,分别为硅酸、氢氧化钠、高氯酸、氢氧化铝.甲+乙→丙+水,丙为盐,丙的水溶液呈碱性,则丙为强碱弱酸盐,则丙为NaAlO2 或Na2SiO3,故答案为:NaAlO2 或Na2SiO3.
点评:本题考查结构、性质与元素、物质的推断、元素周期律等,难度中等,关键清楚元素周期律的变化规律、物质的性质,注意基础知识的掌握与运用.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法中不正确的是( )
| X | Y | ||||
| Z | M | R | |||
| A、元素X和Y可以形成两种以上的气态化合物 |
| B、原子半径的大小顺序为:r(Z)>r(M)>r(R) |
| C、元素的最高价氧化物对应水化物的酸性R强于M |
| D、加热蒸干由元素R和Z形成的化合物的水溶液可以得到该化合物的晶体 |
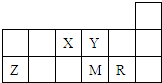 短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法正确的是( )
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法正确的是( )