题目内容
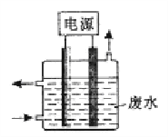
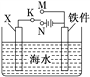
【题目】可用如图装置在铁皮上镀一层锌,以下叙述错误的是( )

A. 电镀前,铁皮可用热碱溶液除油渍,盐酸除铁锈
B. c为铁,d为锌
C. 用含Zn2+的盐配成电解质溶液
D. 电镀时,发生氧化反应和还原反应的都是锌元素
【答案】B
【解析】A项,油渍成份是酯类物质,在碱性条件下易水解,且加热促进酯类物质水解,所以可用热碱溶液除油渍,铁锈的成分是氧化铁,属于碱性氧化物,能与酸反应生成盐和水,所以盐酸能除去铁锈,故A正确;B项,如图根据电流流向可知,a是电源正极,b是电源负极,c是阳极,d是阴极,电镀时,阳极为镀层金属、阴极为镀件,所以c为镀层锌,d为镀件铁,故B错误;C项,电镀时,镀层金属离子的溶液作电镀液,所以含有锌离子的盐溶液为电解质溶液,故C正确;D项,电镀时,阳极上Zn失电子发生氧化反应,阴极上Zn2+得电子发生还原反应,故D正确。

【题目】甲醇是重要的化工原料,又可作为燃料。工业上利用合成气(主要成分为CO、CO2和H2) 在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) ![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-58kJ/mol
CH3OH(g)+H2O(g) △H=-58kJ/mol
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H=+41kJ/mol
CO(g)+H2O(g) △H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(kJ/mol) | a | b | c | d | x |
则x=______。(用含表中字母的代数式表示)
(2)若将lmolCO2和2molH2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应②。测得CH3OH的物质的量随时间的变化如图所示。

①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ_____KⅡ(填“>或“=”或“<”)
②一定温度下,能判断该反应达到化学平衡状态的是______。
a.容器中压强不变
b.甲醇和水蒸气的体积比保持不变
c.v正(H2)=3v逆(CH3OH)
d.2个C=O断裂的同时有3个H-H形成
③若5min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为_____,该温度下的平衡常数为_____,若容器容积不变,下列措施可增加甲醇产率的是____。
a.升高温度 b.使用合适的催化剂 c.充入He d.按原比例再充入CO2和H2