题目内容
已知酒精的沸点常压下为78.6 ℃。工业酒精中含水量较多,制无水乙醇时需要除水。
(1)为除去工业酒精中的水分所加试剂为______________,进行的操作为______________。
(2)为完成上述操作某同学设计了如下两套装置:
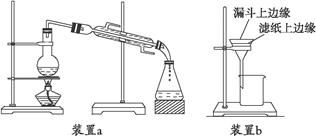
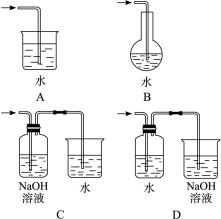
①用“→”标出上图装置a中冷却水进出的方向,用“———”画出装置b中所加液体液面的合适位置。
②你认为应该选用的合适装置是a还是b?_________________(填“a”或“b”)。若选用装置a应注意装置的气密性。那么,检验装置a的气密性的方法是______________________。若选用装置b,有人总结出了进行此操作时注意的三点原则,即“一贴”“二低”“三靠”。那么,它们的具体含义是:
“一贴”,
_______________________________________________________________________。
“二低”,
_______________________________________________________________________。
“三靠”,______________________________________________________________________。
(3)检验上述除水过程中水是否除尽的方法是______________________________________。
(1)为除去工业酒精中的水分所加试剂为______________,进行的操作为______________。
(2)为完成上述操作某同学设计了如下两套装置:

①用“→”标出上图装置a中冷却水进出的方向,用“———”画出装置b中所加液体液面的合适位置。
②你认为应该选用的合适装置是a还是b?_________________(填“a”或“b”)。若选用装置a应注意装置的气密性。那么,检验装置a的气密性的方法是______________________。若选用装置b,有人总结出了进行此操作时注意的三点原则,即“一贴”“二低”“三靠”。那么,它们的具体含义是:
“一贴”,
_______________________________________________________________________。
“二低”,
_______________________________________________________________________。
“三靠”,______________________________________________________________________。
(3)检验上述除水过程中水是否除尽的方法是______________________________________。
(1)生石灰 蒸馏 (2)①
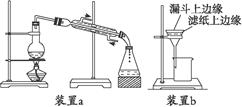
②a 将右端的牛角管插入水槽的水中,然后用手捂住(或轻轻加热)圆底烧瓶一会儿,若牛角管处有气泡生成说明气密性良好 滤纸折好,用水润湿,使滤纸紧贴漏斗内壁 滤纸边缘略低于漏斗边缘,液面低于滤纸边缘 烧杯紧靠玻璃棒,玻璃棒底端紧靠三层滤纸处,漏斗颈的末端紧靠烧杯内壁
(3)用无水硫酸铜

②a 将右端的牛角管插入水槽的水中,然后用手捂住(或轻轻加热)圆底烧瓶一会儿,若牛角管处有气泡生成说明气密性良好 滤纸折好,用水润湿,使滤纸紧贴漏斗内壁 滤纸边缘略低于漏斗边缘,液面低于滤纸边缘 烧杯紧靠玻璃棒,玻璃棒底端紧靠三层滤纸处,漏斗颈的末端紧靠烧杯内壁
(3)用无水硫酸铜
由于酒精的沸点与常压下水的沸点差不多,所以直接蒸馏会混入大量水蒸气,因此,应首先加入生石灰,使水与生石灰反应生成难挥发的氢氧化钙,然后蒸馏即可得到无水乙醇。蒸馏时冷却水应该从低处进入,从高处流出,以便冷凝管内充满水,使冷凝管内的气体充分冷凝。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目

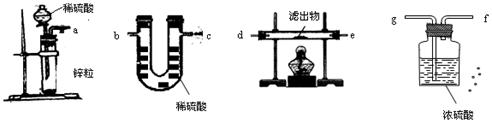
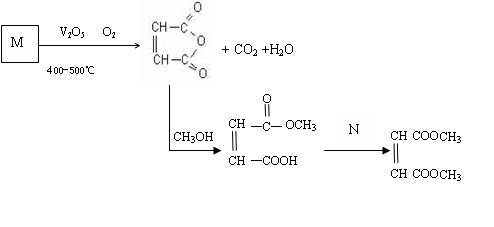 (1)已知烃M的相对分子质量为78,分子内含碳量为92.3%,所有C—H键和碳碳键类型相同,化合物M的化学式为
(1)已知烃M的相对分子质量为78,分子内含碳量为92.3%,所有C—H键和碳碳键类型相同,化合物M的化学式为