题目内容
【题目】车用妄全气囊中反应方程式为BNaN3=2Na+3N2↑,用双桥线标出电子 转移的数目和变化类型,指出氧化剂和还原剂.若要得到标准状况下33.6LN2 , 需要多少克NaN3(写出计算过程),NaN3的密度约为2g/cm3 , 则NaN3的体积约为多少立方厘米.
【答案】解:2NaN3=2Na+3N2↑,Na由+1价降低为0价得电子,N由﹣ ![]() 价升高为0价失电子,转移电子数目为2e﹣ , 所以氧化剂和还原剂都是NaN3 , 双桥线标出电子 转移的数目为
价升高为0价失电子,转移电子数目为2e﹣ , 所以氧化剂和还原剂都是NaN3 , 双桥线标出电子 转移的数目为 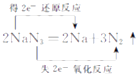 ;
;
由2NaN3=2Na+3N2↑,若要得到标准状况下33.6LN2 , 设需要NaN3为xg,
则
2×65 | 3×22.4 | |
x | 33.6 |
所以 ![]() =
= ![]() ,解得x=75g,则NaN3的体积约为
,解得x=75g,则NaN3的体积约为 ![]() =37.5立方厘米
=37.5立方厘米
答:氧化剂和还原剂都是NaN3 , 双桥线标出电子 转移的数目为 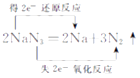 ,若要得到标准状况下33.6LN2 , 设需要NaN375g,体积约为37.5立方厘米.
,若要得到标准状况下33.6LN2 , 设需要NaN375g,体积约为37.5立方厘米.
【解析】2NaN3=2Na+3N2↑,Na由+1价降低为0价得电子,N由﹣ ![]() 价升高为0价失电子,转移电子数目为2e﹣ , 结合化学反应方程式进行分析解答.
价升高为0价失电子,转移电子数目为2e﹣ , 结合化学反应方程式进行分析解答.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目