题目内容
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:HCl>CH4>SiH4
B.氢元素与另一种非金属元素形成的化合物一定是共价化合物
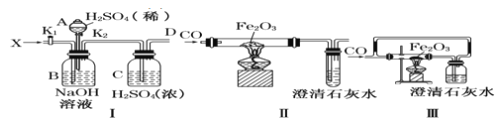
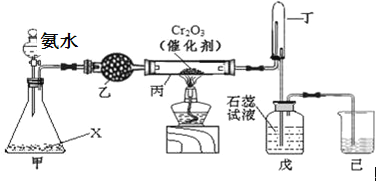
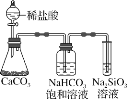
C.如图所示实验不能证明元素的非金属性:Cl>C>Si
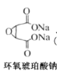
D.用中文“ ![]() ”(ào)命名的第 118 号元素在周期表中位于第七周期 0 族
”(ào)命名的第 118 号元素在周期表中位于第七周期 0 族
【答案】B
【解析】
A.元素非金属性越强对应的简单氢化物越稳定,元素非金属性Cl>C>Si, 所以气态氢化物的稳定性:HCl>CH4>SiH4,A选项正确;
B.H元素可与N元素形成NH4H,为离子化合物,B选项错误;
C.元素对应的最高价含氧酸酸性越强,其非金属性越强,HCl不是最高价含氧酸,所以不能比较Cl、C的非金属性,C选项正确;
D.118号元素的核外有7个电子层,其最外层电子数为8,则118号元素在周期表中位于第七周期0族,D选项正确;
答案选B。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】硫酸工业生产过程中,涉及SO2转化为SO3的反应,某化学研究小组在450 ℃时,在一容积为10 L 的恒容密闭容器中研究该可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),得出的相关数据如表所示:
2SO3(g),得出的相关数据如表所示:
时间/min | n(SO2)/mol | n(O2)/mol | n(SO3)/mol |
0 | 0.200 | 0.100 | 0 |
10 | 0.190 | 0.095 | 0.010 |
15 | 0.160 | 0.080 | 0.040 |
20 | 0.160 | 0.080 | 0.040 |
25 | 0.150 | 0.150 | 0.050 |
根据表中数据,下列判断正确的是
A. 0~10 min内的反应速率可表示为v(SO2)=0.010 mol/(L·min)
B. 15~20 min内,正、逆反应速率不相等
C. 工业上常用增加SO2的量来提高O2的转化率
D. 20~25 min内,数据变化的原因可能是增加了O2的物质的量