题目内容
【题目】已知,某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL0.1mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法正确的是
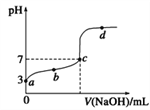
A. a点表示溶液中c(CH3COO-)约为10-3 mol/L
B. b点表示的溶液中c(CH3COO-)< c(Na+)
C. c点表示CH3COOH和NaOH恰好反应完全
D. b、d点表示的溶液中 的值不相等
的值不相等
【答案】A
【解析】A、a点是c(H+)=10-3mol/L,由于醋酸为弱酸,酸能抑制水的电离,醋酸的电离远远大于水的电离,所以溶液中氢离子浓度近似等于醋酸根离子浓度,即c(CH3COO-)约为10-3mol/L,选项A正确;B、溶液中一定满足电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),b点时,溶液显酸性,c(H+)>c(OH-),则有c(CH3COO-)>c(Na+),选项B错误;C、醋酸和氢氧化钠反应生成醋酸钠,醋酸钠是强碱弱酸盐,其水溶液呈碱性,当酸碱恰好反应时溶液应该呈碱性,但c点溶液呈中性,说明酸过量,选项C错误;D、CH3COOH的电离平衡常数K=  ,b点、d点时溶液的温度没有变化,所以电离平衡常数不变,应该相等,选项D错误。答案选A。
,b点、d点时溶液的温度没有变化,所以电离平衡常数不变,应该相等,选项D错误。答案选A。

【题目】氮化镁(Mg3N2)在工业上应用广泛,通常条件下为黄绿色粉末,极易与水反应,常用作接触媒。
I.氮化镁的制备 下面是甲、乙两位学生提出的制备氮化镁的实验方案示意图(实验前系统内的空气已排除。图中箭头表示气体的流向)。
甲. ![]()
乙. ![]()
(1)Mg3N2的电子式为___________,甲同学的实验方案不能顺利制得氮化镁,原因为________ (用化学方程式表示)。
(2)乙同学方案中NaOH固体的作用为_____________________________________________。
(3)丙同学利用空气中含有大量N2的事实,用以下装置设计了另外一种制备氮化镁的方案 (夹持装置略去):

①按气流由左到右的方向,上述装置合理的连接顺序为____________(填接口字母);
②装置B的作用为___________,装置D的作用为__________________________。
Ⅱ.定性分析产物
操作步明 | 实验现象 | 解释原因 |
取少量产品于试管中,加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | (4)反应的化学方程式为___________ |
. | ||
弃去上层淸液,加入足量稀盐酸 | 观察到固体全部溶解,且有气泡冒出 | (5)气泡冒出的原因为_____________ |
Ⅲ.定量测定氮化镁纯度
i.称取4.0 g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00 mol/L盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00 mL稀释后的溶液,用0.2 mol/L NaOH标准溶液滴定过量的盐酸,达到终点时消耗标准溶液25.00 mL。
(6)产物中氮化镁的质量分数为_______________。

