题目内容
已知:H2O(g)=H2O(l)ΔH=Q1kJ·mol-1
C2H5OH(g)=C2H5OH(l)ΔH=Q2kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH=Q3kJ·mol-1
若使46g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
A.(Q1+Q2+Q3) kJ B.0.5(Q+Q2+Q3) kJ
C.(0.5Q1-1.5Q2+0.5Q3) kJ D.(Q2-3Q1-Q3)kJ
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.利用下图装置探究温度对氨气还原Fe2O3的影响(固定装置略).
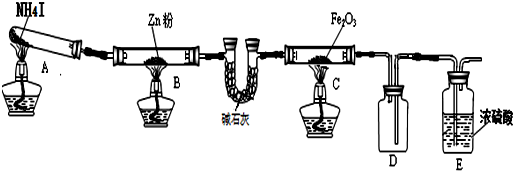
完成下列填空:
(1)实验时A中有大量紫红色的烟气,烟气的主要成份是NH3、H2、I2、HI,在上图装置中,碱石灰的作用是吸收混合气体中的HI;
(2)装置B中,Zn会与I2发生反应,其反应化学方程式Zn+I2═ZnI2
-;
(3)按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置C加热,反应产物均为黑色粉末 (纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
?乙组得到的黑色粉末是Fe;?步骤1甲组中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O;
(4)若装置C中反应后的固体是Fe2O3和FeO组成的混合物.为确定其组成,取样品7.84克,在加热 条件下通入足量的氨气,完全反应后,停止加热,Fe2O3和FeO都被还原为Fe,反应管中铁粉冷却后,称得质量为5.6克,则混合物中Fe2O3和FeO的物质的量之比为2:1.

完成下列填空:
(1)实验时A中有大量紫红色的烟气,烟气的主要成份是NH3、H2、I2、HI,在上图装置中,碱石灰的作用是吸收混合气体中的HI;
(2)装置B中,Zn会与I2发生反应,其反应化学方程式Zn+I2═ZnI2
-;
(3)按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置C加热,反应产物均为黑色粉末 (纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无明显变化 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
(4)若装置C中反应后的固体是Fe2O3和FeO组成的混合物.为确定其组成,取样品7.84克,在加热 条件下通入足量的氨气,完全反应后,停止加热,Fe2O3和FeO都被还原为Fe,反应管中铁粉冷却后,称得质量为5.6克,则混合物中Fe2O3和FeO的物质的量之比为2:1.
14.粘土胶体溶液中,粘土粒子带负电,为了使粘土粒子凝聚,下列物质中用量最少但最有效的电解质是( )
| A. | Na3PO4 | B. | A12(SO4)3 | C. | BaCl2 | D. | K2SO4 |


 V2=50ml)。下列叙述正确的是( )
V2=50ml)。下列叙述正确的是( )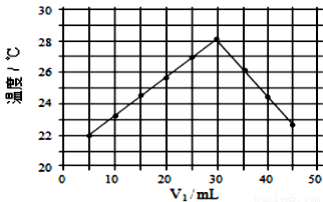
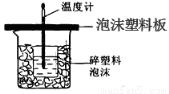
 等”);所求中和热的数值会______________(填“相等”或 “不相等”)。
等”);所求中和热的数值会______________(填“相等”或 “不相等”)。
 C(g)+2D(g);经5min达到平衡, 测得压强减小了10%,下列说法中正确的是
C(g)+2D(g);经5min达到平衡, 测得压强减小了10%,下列说法中正确的是 )通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
)通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。 O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1
O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1