题目内容
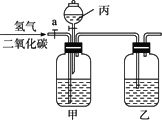
实验室现有水、浓硫酸和氢氧化钠溶液及一些常用的仪器。如要用下图所示装置对氢气和二氧化碳的混合气体进行分离和干燥,你认为:
(1)甲中应盛放的试剂是_________________。
(2)乙中应盛放的试剂是_________________。
(3)首先打开活塞a,可分离出的气体是______,发生反应的化学方程式:_________________。
(4)分离出另一种气体的方法是:关闭活塞a,从漏斗丙中加入试剂_________________。
解析:(1)甲中试剂吸收CO2,所以放入NaOH溶液;乙中试剂干燥H2(对应题目要求“分离和干燥”),所以用浓H2SO4。
(2)操作:从a通入混合气,CO2+2NaOH![]() Na2CO3+H2O
Na2CO3+H2O
H2从乙导管口逸出。关闭a,由丙中加入浓H2SO4、Na2CO3+H2SO4![]() Na2SO4+CO2↑+H2O
Na2SO4+CO2↑+H2O
CO2气再经乙干燥即可。
答案:(1)NaOH溶液 (2)浓H2SO4 (3)H2 CO2+2NaOH![]() Na2CO3+H2O (4)浓H2SO4
Na2CO3+H2O (4)浓H2SO4

练习册系列答案
相关题目
 工业上常用铁质容器盛装冷浓硫酸.某兴趣小组的同学发现:将一定量的铁钉与浓硫酸加热时,观察到铁钉完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.10mol/L KI溶液、新制氯水、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.
工业上常用铁质容器盛装冷浓硫酸.某兴趣小组的同学发现:将一定量的铁钉与浓硫酸加热时,观察到铁钉完全溶解,并产生大量气体.实验室现有下列试剂:0.01mol/L 酸性KMnO4溶液、0.10mol/L KI溶液、新制氯水、淀粉溶液、蒸馏水.请你协助他们探究所得溶液和气体的成分.