题目内容
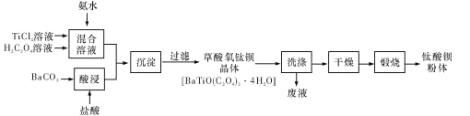
【题目】钛酸钡粉体是电子陶瓷元器件的重要基础原料,其制备工艺流程如下图所示:
(1)镁的碳化物常见的有MgC2和Mg2C3两种,它们均极易与水发生反应。写出MgC2发生水解反应的化学方程式:_____;Mg2C3的电子式为_____。
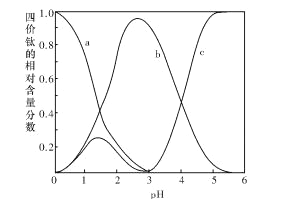
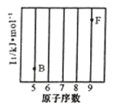
(2)“混合溶液”环节,钛元素在不同pH下主要以种形式存在,如上图所示。实际制备工艺中,先用氨水调节混合溶液的pH于2.5~3之间,再进行“沉淀”,则上图中曲线a对应钛的形式为______填化学符号);写出“沉淀”时的离子方程式:_____。
(3)草酸氧钛钡晶体经蒸馏水数次洗涤后,证明它已被洗涤干净的实验方案为_____。
(4)工业上TiCl4和BaCO3通常用如下方法制备:
①先将金红石(TiO2)与过量焦炭混合,再通入Cl2)并加热到900℃制取TiCl4。请写出该法制备TiCl4的化学方程式:_____。
②BaCO3是将重晶石(主要成分为BaSO4)浸泡在Na2C03溶液中足够长时间来制备。请问Na2CO3溶液的浓度至少要大于_____mol/L才能开始转化。(已知常温下:![]()
![]() ,略CO32-的水解)。
,略CO32-的水解)。
【答案】(1)MgC2+2H2O=Mg(OH)2![]() +C2H2
+C2H2![]() ;(2)
;(2) ![]() (3)TiOC2O4(4) TiO(C2O4)22-+ Ba2++ 4H2O = BaTiO(C2O4)2·4H2O↓(5)取最后一次洗涤液少量于试管中,向其中滴加AgNO3溶液,无白色沉淀生成证明草酸氧钛钡已被洗涤干净(6)TiO2+2C+2Cl2
(3)TiOC2O4(4) TiO(C2O4)22-+ Ba2++ 4H2O = BaTiO(C2O4)2·4H2O↓(5)取最后一次洗涤液少量于试管中,向其中滴加AgNO3溶液,无白色沉淀生成证明草酸氧钛钡已被洗涤干净(6)TiO2+2C+2Cl2![]() TiCl4+2CO(7)2.58×10-4
TiCl4+2CO(7)2.58×10-4
【解析】
(1)MgC2水解生成氢氧化镁和乙炔,反应的方程式为:MgC2+2H2O=Mg(OH)2![]() +C2H2
+C2H2![]() ; Mg2C3属于离子化合物,其电子式为
; Mg2C3属于离子化合物,其电子式为![]() ;
;
故答案为:MgC2+2H2O=Mg(OH)2![]() +C2H2
+C2H2![]() ;
;![]() ;
;
(2)据“沉淀”时生成草酸氧钛钡晶体中含有TiO(C2O4)22-(即b微粒),随着氨水的不断加入C2O42-浓度逐渐增大的趋势可以判断a对应钛的形式为TiOC2O4。根据沉淀的化学式即可写出离子方程式TiO(C2O4)22-+ Ba2++ 4H2O = BaTiO(C2O4)2+4H2O↓。
(3)根反应据过程知洗涤液中可能含有Cl—,所以取最后一次洗涤液少量于试管中,向其中滴加AgNO3溶液,如无白色沉淀生成,证明草酸氧钛钡已被洗涤干净。答案: 取最后一次洗涤液少量于试管中,向其中滴加AgNO3溶液,如无白色沉淀生成,证明草酸氧钛钡已被洗涤干净 。
(4)①由足量焦炭和Cl2反应判断产物为TiCl4和CO,所以化学方程式为TiO2+2C+2Cl2![]() TiCl4+2CO。答案:TiO2+2C+2Cl2
TiCl4+2CO。答案:TiO2+2C+2Cl2![]() TiCl4+2CO 。
TiCl4+2CO 。
②设BaSO4饱和溶液中c(Ba2+)和c(SO42-)均为xmol·L-1,由KSP(BaSO4)=c(Ba2+)c(SO42-)知:x2=1.0×10-10(mol·L-1)2,可求出c(Ba2+)=1.0×10-5mol·L-1。重晶石转化为碳酸钡,需满足Q(BaCO3)=c(Ba2+)c(CO32-)=1.0×10-5mol·L-1×c(CO32-)>KSP(BaCO3),则c(CO32-)>2.58×10-9(mol·L-1)2÷1.0×10-5mol·L-1=2.58×10-4mol·L-1,所以Na2CO3 溶液的浓度至少要大于2.58×10-4mol/L 才能开始转化。答案:2.58×10-4。