题目内容
某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO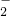 、S2-、CO32-、SO32-、SO
、S2-、CO32-、SO32-、SO .现取该溶液进行有关实验,实验结果如下图所示:
.现取该溶液进行有关实验,实验结果如下图所示:
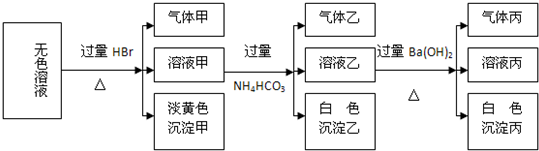
(1)沉淀甲是______,生成沉淀的离子方程式______.
(2)沉淀乙是______,由溶液甲生成沉淀乙的离子方程式______.
(3)沉淀丙是______.
(4)综合上述信息,可以肯定存在的离子有______.
解:由无色溶液加HBr产生淡黄色沉淀,则沉淀甲为S,则发生2S2-+SO32-+6H+=3S↓+3H2O,一定存在S2-、SO32-;溶液甲与过量碳酸氢铵反应,则沉淀乙为Al(OH)3,气体乙为二氧化碳,溶液乙中加过量氢氧化钡反应生成白色沉淀丙应为BaCO3,气体丙为氨气,Ag+、Ba2+、Al3+与S2-、SO32-不能共存,则不存在,由电荷守恒可知,一定存在的阳离子为Na+,一定存在的阴离子为S2-、SO32-、AlO2-,
(1)由上述分析可知,沉淀甲为S,生成沉淀的离子反应为2S2-+SO32-+6H+=3S↓+3H2O,故答案为:S;2S2-+SO32-+6H+=3S↓+3H2O;
(2)沉淀乙为Al(OH)3,生成沉淀乙的离子反应为Al3++3HCO3-=Al(OH)3↓+3CO2↑,故答案为:Al(OH)3;Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(3)原溶液中有可能有硫酸根离子,溶液乙中含碳酸氢根离子,则沉淀丙为BaCO3,可能有BaSO4,在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3 外还有BaSO4;若全部溶解,则仅有BaCO3,
故答案为:BaCO3,可能有BaSO4,在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3外还有BaSO4,若全部溶解,则仅有BaCO3;
(4)肯定存在的离子有Na+、S2-、SO32-、AlO2-,故答案为:Na+、S2-、SO32-、AlO2-.
分析:由无色溶液加HBr产生淡黄色沉淀,则沉淀甲为S,则发生2S2-+SO32-+6H+=3S↓+3H2O,一定存在S2-、SO32-;溶液甲与过量碳酸氢铵反应,则沉淀乙为Al(OH)3,气体乙为二氧化碳,溶液乙中加过量氢氧化钡反应生成白色沉淀丙应为BaCO3,气体丙为氨气,然后结合离子的共存来分析.
点评:本题考查离子的共存及离子反应,利用流程及离子之间的反应推断出存在离子是解答的关键,注意过量离子及电荷守恒的应用,题目难度中等.
(1)由上述分析可知,沉淀甲为S,生成沉淀的离子反应为2S2-+SO32-+6H+=3S↓+3H2O,故答案为:S;2S2-+SO32-+6H+=3S↓+3H2O;
(2)沉淀乙为Al(OH)3,生成沉淀乙的离子反应为Al3++3HCO3-=Al(OH)3↓+3CO2↑,故答案为:Al(OH)3;Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(3)原溶液中有可能有硫酸根离子,溶液乙中含碳酸氢根离子,则沉淀丙为BaCO3,可能有BaSO4,在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3 外还有BaSO4;若全部溶解,则仅有BaCO3,
故答案为:BaCO3,可能有BaSO4,在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3外还有BaSO4,若全部溶解,则仅有BaCO3;
(4)肯定存在的离子有Na+、S2-、SO32-、AlO2-,故答案为:Na+、S2-、SO32-、AlO2-.
分析:由无色溶液加HBr产生淡黄色沉淀,则沉淀甲为S,则发生2S2-+SO32-+6H+=3S↓+3H2O,一定存在S2-、SO32-;溶液甲与过量碳酸氢铵反应,则沉淀乙为Al(OH)3,气体乙为二氧化碳,溶液乙中加过量氢氧化钡反应生成白色沉淀丙应为BaCO3,气体丙为氨气,然后结合离子的共存来分析.
点评:本题考查离子的共存及离子反应,利用流程及离子之间的反应推断出存在离子是解答的关键,注意过量离子及电荷守恒的应用,题目难度中等.

练习册系列答案
相关题目
