题目内容
14.下列叙述正确的是( )| A. | 直径介于1~100nm之间的微粒称为胶体 | |
| B. | 用过滤的方法可以将胶体和溶液分离 | |
| C. | 利用丁达尔效应可以区别溶液和胶体 | |
| D. | 胶体区别于其他分散系的本质特征是丁达尔效应 |
分析 A、当分散剂是水或其它溶液时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm);
B、胶体和溶液都能透过滤纸;
C、胶体具有丁达尔效应而溶液不具备;
D、胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径的大小;
解答 解:A、当分散剂是水或其它溶液时,分散质粒子直径大小在1nm~100nm之间的是胶体,故A错误;
B、胶体和溶液都能透过滤纸,不能用过滤的方法分离胶体和溶液,故B错误;
C、胶体具有丁达尔效应而溶液不具备,可以据此区别溶液和胶体,故C正确;
D、胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径10-9-10-7m之间,故D错误;
故选C.
点评 本题考查胶体的特性以及溶液和胶体的本质区别,熟悉胶体的性质是解答的关键,题目较简单.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
4.可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有6个N-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④恒温恒容时,密度保持不变 ⑤NH3%不再改变
⑥2υ正(H2)=3υ逆(NH3)
⑦温度不再改变
⑧N2、H2、NH3物质的量之比为1:3:2.
①一个N≡N键断裂的同时,有6个N-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④恒温恒容时,密度保持不变 ⑤NH3%不再改变
⑥2υ正(H2)=3υ逆(NH3)
⑦温度不再改变
⑧N2、H2、NH3物质的量之比为1:3:2.
| A. | ①③⑤⑥⑦ | B. | ①②③⑤⑥⑦ | C. | ①③④⑤⑥⑦ | D. | 全部 |
5.下列说法正确的是( )
| A. | 煤的气化、液化是物理变化,煤的干馏是化学变化 | |
| B. | C60、液氯是单质,HD、干冰是化合物,NO2是酸性氧化物 | |
| C. | 烟、雾属于胶体,能产生丁达尔效应 | |
| D. | 可用热的饱和碳酸钠溶液除去金属表面的石蜡 |
9.下列各组中的两稀溶液间的反应,可以用同一个离子方程式来表示的是( )
| A. | HCl与Na2CO3;HNO3与KHCO3 | B. | BaCl2与Na2SO4;Ba(OH)2与CuSO4 | ||
| C. | HCl与KOH;H2SO4与Ba(OH)2 | D. | H2SO4与NaHCO3;NaHSO4与KHCO3 |
15.氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等.某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数.反应的化学方程式:2NH3(g)+CO2(g) $?_{分解}^{制备}$NH2COONH4(s).请按要求回答下列问题:
(1)请在图1方框内画出用浓氨水与生石灰制取氨气的装置简图.
(2)制备氨基甲酸铵的装置如图2所示.生成的氨基甲酸铵小晶体悬浮在四氯化碳中.
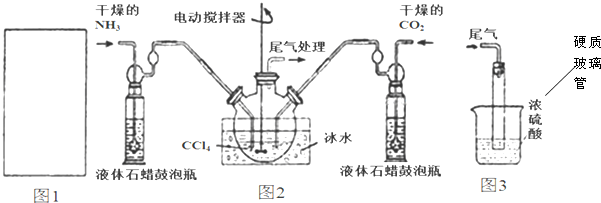
①从反应后的混合物中分离出产品的实验方法是过滤(填操作名称).
②图3中浓硫酸的作用是吸收未反应的氨气,防止空气中的水蒸气进入反应器使氨基甲酸铵水解.
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡.实验测得不同温度下的平衡数据列于下表:
①下列选项可以判断该分解反应达到平衡的是AC.
A.密闭容器内混合气体的压强不变
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变△H>0(填“>”、“=”或“<”),25.0℃时分解平衡常数的值=1.6384×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”,“减少”或“不变”).
(1)请在图1方框内画出用浓氨水与生石灰制取氨气的装置简图.
(2)制备氨基甲酸铵的装置如图2所示.生成的氨基甲酸铵小晶体悬浮在四氯化碳中.

①从反应后的混合物中分离出产品的实验方法是过滤(填操作名称).
②图3中浓硫酸的作用是吸收未反应的氨气,防止空气中的水蒸气进入反应器使氨基甲酸铵水解.
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡.实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.密闭容器内混合气体的压强不变
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变△H>0(填“>”、“=”或“<”),25.0℃时分解平衡常数的值=1.6384×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”,“减少”或“不变”).
16.下列有关叙述正确的是( )
| A. |  如图所示,测定中和反应的反应热时,大小两烧杯间填满碎泡沫塑料的作用是固定小烧杯 如图所示,测定中和反应的反应热时,大小两烧杯间填满碎泡沫塑料的作用是固定小烧杯 | |
| B. | 若用50 mL 0.55 mol•L-1的氢氧化钠溶液,分别与50 mL 0.50 mol•L-1的盐酸和50 mLA0.50 mol•L-1的硝酸充分反应,两反应测定的反应热不相等 | |
| C. | 实验时需要记录初始温度T1 和最高温度T2 | |
| D. | 做一次实验根据公式即可得出中和反应的反应热 |